Атомы, как основные строительные блоки материи, состоят из заряженных частиц - протонов, нейтронов и электронов. Существует фундаментальное понятие, связанное с атомами - электронейтральность. Оно означает, что атом в целом не имеет электрического заряда. Однако, почему ядро атома имеет положительный заряд, в то время как количество протонов равно количеству электронов в атоме?
Для понимания этого вопроса необходимо знать, что протоны и электроны обладают противоположными зарядами, протон имеет положительный заряд (+1), а электрон - отрицательный заряд (-1). Изначально, атом является нейтральным, так как количество протонов, определяющих положительный заряд ядра, равно количеству электронов, определяющих отрицательный заряд вокруг ядра. Это объясняется тем, что атом стремится достичь электронейтральности, в которой притяжение протонов и электронов друг к другу сбалансировано.
Однако в реальности, некоторые атомы могут стать ионами, то есть атомами с электрическим зарядом, когда количество протонов и электронов в атоме не совпадает. При этом, ионы могут иметь положительный (катионы) или отрицательный (анионы) заряды. Такой дисбаланс обычно происходит из-за взаимодействия атомов с другими частицами или из-за добавления или удаления электронов из атома.
Заряд ядра атома и электронейтральность: причины и объяснение
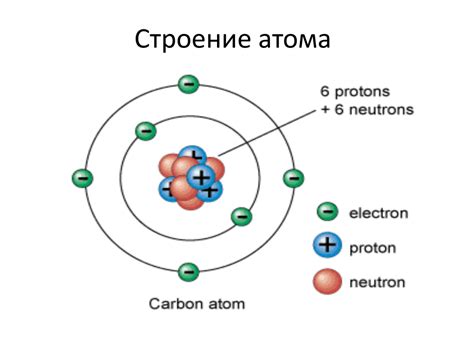
Заряд ядра атома
Ядро атома содержит протоны и нейтроны. Протоны имеют положительный электрический заряд, а нейтроны не имеют заряда и являются электрически нейтральными. Заряд ядра определяется количеством протонов в нем.
Электронейтральность
Атомы стремятся быть электронейтральными, то есть иметь равное количество положительных и отрицательных зарядов. Электроны находятся в облаке вокруг ядра, и их количество обычно равно количеству протонов в ядре.
Причины заряда ядра и электронейтральности
Заряд ядра определяется под влиянием сильной ядерной силы, которая притягивает протоны друг к другу, преодолевая их электростатическое отталкивание. Нейтроны, не имеющие заряд, также притягиваются сильной ядерной силой к протонам и поддерживают ядро стабильным.
Атомы становятся электронейтральными по причине силы притяжения между положительно заряженными протонами и отрицательно заряженными электронами. Электроны находятся в облаке, которое формирует электронную оболочку вокруг ядра. Количество электронов в облаке равно количеству протонов в ядре, что обеспечивает электронейтральность атома.
Причины заряда ядра атома
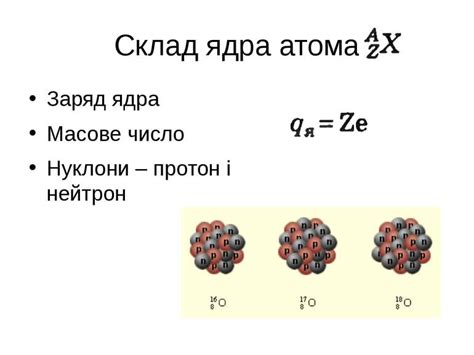
Если в атоме присутствуют электроны, они обладают отрицательным зарядом. Однако положительный заряд ядра уравновешивается отрицательным зарядом электронов, что делает атом электронейтральным. Количество электронов в атоме равно количеству протонов.
Заряд ядра атома играет важную роль в химических реакциях, взаимодействии атомов и молекул. Например, заряд ядра определяет силу притяжения или отталкивания между атомами, что влияет на свойства и химическую активность вещества.
Таким образом, причинами заряда ядра атома являются присутствие протонов с положительным зарядом и равновесное количество отрицательно заряженных электронов, что делает атом электронейтральным и обуславливает его химические свойства.
Электронейтральность атома
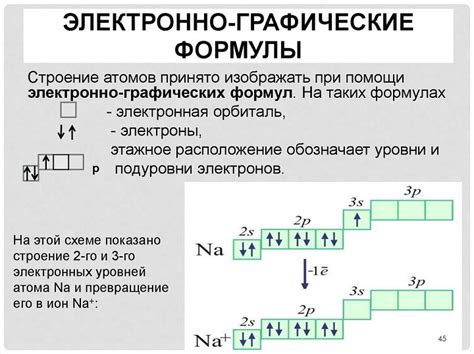
Электроны – элементарные частицы, обладающие отрицательным электрическим зарядом. Они находятся в электронных оболочках вокруг ядра атома и принимают участие в химических реакциях, обеспечивая связи между атомами в молекулах. Протоны – другие элементарные частицы, но уже с положительным зарядом. Вместе с неутронами они образуют ядро атома.
Протоны и электроны – основные элементы, формирующие атом. Их количество может быть разным в разных атомах. Однако, чтобы атом был электрически нейтральным, количество протонов должно быть равным количеству электронов. В противном случае, если число протонов и электронов различается, атом будет иметь неизменный положительный или отрицательный заряд.
Примеры:
1. Высыпь батарейки – атомы некоторых металлов, таких как цинк и медь, имеют электронейтральную структуру. В цинке 30 электронов и 30 протонов, а в меди – 29 электронов и 29 протонов. Поэтому они обладают нулевым электрическим зарядом.
2. Ион кислорода воды – водная молекула состоит из одного атома кислорода и двух атомов водорода. Атом кислорода имеет 8 протонов и 8 электронов, что обеспечивает его электронейтральность. Однако, в процессе химической реакции кислород может получить или потерять электроны, образуя отрицательно или положительно заряженные ионы.
3. Йодид натрия – в этом соединении йод имеет отрицательный заряд, поскольку его атому не хватает одного электрона для полного заполнения электронной оболочки. Атом натрия, напротив, имеет один электрон лишний, поэтому он положительно заряжен. Соединение нейтрализуется благодаря образованию кристаллической решетки, в которой ионы йода и натрия образуют нейтральные пары.
Таким образом, электронейтральность атома связана с равным количеством электронов и протонов. Это позволяет атому быть стабильным и электрически нейтральным.



