В химии алкены – это класс органических соединений, содержащих двойную связь между атомами углерода. Одним из интересных фактов об алкенах является то, что их массовая доля углерода всегда одинакова независимо от их молекулярной формулы и структуры.
Прежде всего, необходимо понять, что массовая доля углерода в химическом соединении рассчитывается как отношение массы углерода к общей массе соединения, умноженное на 100%. Когда дело доходит до алкенов, внешний вид разных алкенов может значительно отличаться. Однако внутри молекулы все алкены имеют одинаковое число атомов углерода и водорода.
Таким образом, массовая доля углерода в алкенах одинакова, потому что все алкены содержат одинаковое количество углерода в своих молекулах. Это связано с тем, что химические связи между атомами углерода и атомами водорода не влияют на порядок межатомных расстояний и, следовательно, на массовую долю углерода.
Структура алкенов
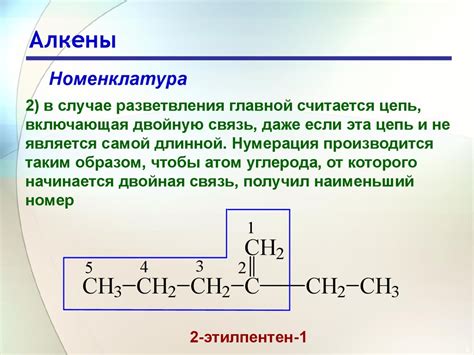
Двойная связь в алкенах состоит из одной σ-связи (сигма-связи) и одной π-связи (пи-связи), где сигма-связь является ковалентной связью, а пи-связь формируется из перекрывающихся п-орбиталей. Это делает алкены более реакционноспособными по сравнению с алканами, которые имеют только σ-связи.
Структура алкенов также позволяет иметь геометрические изомеры – изомеры, которые отличаются пространственным расположением атомов, но имеют одинаковую молекулярную формулу. Например, этилен и пропен имеют геометрический изомеризм, где двойная связь может быть расположена either в плоскости молекулы (cis-изомер) или в разные стороны от плоскости молекулы (trans-изомер).
Реакционная способность алкенов, их физические свойства и важные биологические функции обычно зависят от их структуры, включая длину цепи атомов углерода, расположение двойной связи и наличие функциональных групп. Поэтому понимание структуры алкенов является важным для изучения их химических свойств и использования в различных областях науки и техники.
Чем отличаются алкены от алканов

Главное отличие алкенов от алканов состоит в том, что алкены содержат хотя бы одну двойную связь между углеродными атомами. В то время как алканы, с другой стороны, содержат только одинарные связи между атомами углерода.
Двойная связь в алкенах обладает уникальными химическими свойствами и способствует возможности использования алкенов во множестве химических реакций. Например, они более реакционноспособны и более подвержены аддиционным реакциям, чем алканы.
Другие отличия между алканами и алкенами включают разность в названии и физических свойствах. Например, алкены имеют названия, оканчивающиеся на "-ен", а алканы - на "-ан". Алкены также имеют более низкую точку кипения и плотность по сравнению с алканами.
Однако структура алкенов очень похожа на структуру алканов, за исключением наличия двойной связи. Их общая формула CnH2n позволяет определить массовую долю углерода в алкенах, которая всегда одинакова. Это свойство делает ее одним из ключевых отличий между алканами и алкенами.
Связь между структурой и массовой долей углерода

Массовая доля углерода в молекуле алкена определяется следующим образом: она равна отношению массы углерода к молекулярной массе всей молекулы и выражается в процентах. Таким образом, массовая доля углерода позволяет оценить, насколько богат углеродом данный органический соединение.
Стоит отметить, что массовая доля углерода во всех алкенах одинакова и составляет 85,7%. Все алкены имеют общую формулу CₙH₂ₙ, где n - количество атомов углерода в молекуле.
Это обусловлено тем, что каждая двойная связь в алкене состоит из одной сигма-связи и одной пи-связи. Атомы углерода в молекуле алкена связаны между собой только с помощью этих связей, и ни одна из них не принимает участие в связи с другими элементами.
Таким образом, массовая доля углерода во всех алкенах остается постоянной, что делает ее универсальным индикатором и отличительной характеристикой этого класса органических соединений.
Формула для определения массовой доли углерода

Массовая доля углерода в алкенах определяется по простой формуле, основанной на химическом составе алкенов.
Для определения массовой доли углерода в алкене необходимо знать количество углеродных атомов и молекулярную массу соответствующего алкена.
Массовая доля углерода (C) в алкене может быть рассчитана по следующей формуле:
C% = (2 * кол-во углеродных атомов * молекулярная масса углерода) / молекулярная масса алкена * 100%
В формуле, 2 умножается на количество углеродных атомов, поскольку каждая двойная связь, характерная для алкенов, состоит из двух углеродных атомов.
Результат расчета массовой доли углерода в алкене будет выражен в процентах. Эта доля показывает, какую долю в молекуле алкена занимают углеродные атомы.
Знание массовой доли углерода в алкенах помогает химикам и исследователям более точно определять свойства и реакционную способность данных соединений, что является важным фактором в дальнейших исследованиях.
Почему массовая доля углерода одинакова

Алкены представляют собой органические соединения, содержащие двойную связь между атомами углерода. Молекула алкена состоит из серии углеродных атомов, соединенных друг с другом и с водородом. Каждый углеродный атом имеет валентность, равную четырем. Один из его связующих атомов может быть атомом водорода, а остальные - другими углеродными атомами. Молекулы алкенов могут быть линейными, ветвистыми или кольцевыми.
Такое строение молекулы алкена обусловливает одинаковую массовую долю углерода во всех его разновидностях. При определении массовой доли углерода в алкене необходимо учитывать количество атомов углерода и общее количество атомов в молекуле. Поскольку каждый углеродный атом имеет четыре связи, для удовлетворения этого требования и образования двойной связи с соседним атомом углерода, в молекуле алкена обязательно должно быть два углеродных атома. Соответственно, наличие двойной связи исключает наличие тройной или одинарной связи и количество углеродных атомов не может быть меньше двух или больше, чем это необходимо для удовлетворения валентности атомов.
Таким образом, массовая доля углерода одинакова во всех алкенах из-за особенностей их строения. Наличие двойной связи между атомами углерода в каждой молекуле алкена гарантирует, что массовая доля углерода будет одинакова вне зависимости от количества атомов углерода в молекуле.
Примеры алкенов с одинаковой массовой долей углерода
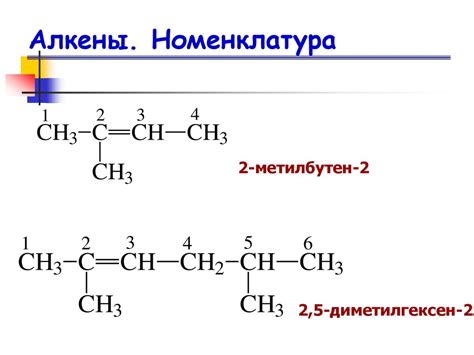
Массовая доля углерода в алкенах определяется числом атомов углерода в молекуле, относительно общего числа атомов.
Примером алкена с одинаковой массовой долей углерода может служить этилен, химическая формула которого C2H4. В этой молекуле есть два атома углерода и шесть атомов водорода. Молекула этилена состоит на 33% из атомов углерода.
Еще одним примером алкена с одинаковой массовой долей углерода является пропилен, C3H6. В молекуле пропилена содержится три атома углерода и шесть атомов водорода. Атомы углерода составляют также 33% от общего числа атомов в молекуле.
Таким образом, этилен и пропилен являются примерами алкенов с одинаковой массовой долей углерода, поскольку они оба содержат по два атома углерода и шесть атомов водорода.
Роль массовой доли углерода в свойствах алкенов

Массовая доля углерода в алкенах позволяет определить количество атомов углерода в отношении общего числа атомов в молекуле. Этот параметр напрямую влияет на физические и химические свойства алкенов.
Чем больше массовая доля углерода в алкене, тем более устойчивой и инертной является его молекула. Углерод, образующий основу алкена, обладает способностью образовывать четыре ковалентные связи одновременно, что делает его молекулы наиболее стабильными и малоактивными в химических реакциях.
Вместе с тем, массовая доля углерода также влияет на физические свойства алкенов. Более высокая массовая доля углерода обычно приводит к более высоким температурам плавления и кипения алкенов, так как углеродные атомы обладают высокой связностью между собой.
Также, массовая доля углерода в алкенах определяет основные классы их соединений. Например, алкены с двумя атомами углерода называются этиленами, с тремя – пропиленами, с четырьмя – бутенами и так далее. Это помогает классифицировать алкены и определять их свойства на основе количества углеродных атомов в молекуле.
Обладая разнообразными свойствами и применением в различных отраслях науки и промышленности, алкены являются важными органическими соединениями. Массовая доля углерода играет ключевую роль в их свойствах и открывает возможность для изучения их разнообразных аспектов и применений.
| Количество атомов углерода | Примеры алкенов |
|---|---|
| 2 | этилен |
| 3 | пропилен |
| 4 | бутен |
| 5 | пентен |
| ... | ... |
Зависимость между массовой долей углерода и физическими свойствами алкенов

Это обусловлено особенностями структуры алкенов. Все алкены содержат два группированных атома углерода, связанных между собой двойной связью. Таким образом, массовая доля углерода в алкене всегда составляет 66,67%.
Зависимость массовой доли углерода от физических свойств алкенов является важным аспектом и позволяет предсказывать некоторые химические свойства этих соединений. Например:
- Увеличение массовой доли углерода ведет к повышению температуры кипения алкенов. Это связано с увеличением числа атомов углерода, которые образуют взаимодействия с молекулами других веществ.
- Повышение массовой доли углерода также увеличивает плотность алкенов, так как большее количество атомов углерода создает более компактную структуру.
- Массовая доля углерода также может влиять на растворимость алкенов в различных растворителях. Большее количество атомов углерода может увеличить гидрофобность молекулы и, следовательно, снизить ее растворимость в полярных растворителях.
Таким образом, массовая доля углерода в алкенах является фундаментальным параметром, который определяет их физические свойства и химическую активность. Понимание этой зависимости может быть полезным инструментом для изучения и прогнозирования свойств алкенов в химических реакциях и промышленных процессах.
Зависимость между массовой долей углерода и химическими свойствами алкенов
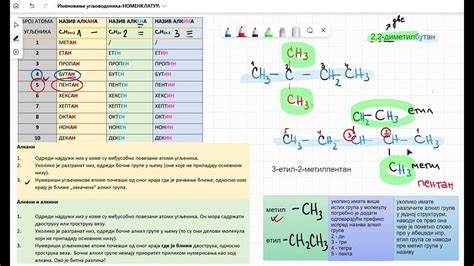
Массовая доля углерода одинакова во всех алкенах из-за особенностей их химической структуры. Алкены представляют собой органические соединения, которые содержат две связи между атомами углерода, называемые двойными связями. Такая структура позволяет алкенам иметь общую формулу CnH2n, где "n" представляет число углеродных атомов в молекуле.
Из-за наличия двойных связей и удвоенного количества атомов водорода по сравнению с числом углеродных атомов, массовая доля углерода в алкенах всегда остается постоянной. Это является основой для классификации и идентификации алкенов в химических реакциях и различных процессах.
Такая структурная особенность алкенов также влияет на их химические свойства. Одно из ключевых свойств алкенов - их реакционная способность. Двойные связи алкенов могут быть разорваны и превращены в одиночные связи, что создает возможность для различных химических превращений.
Массовая доля углерода в алкенах также имеет значение при определении их физических свойств, таких как температура плавления и кипения. По мере увеличения числа углеродных атомов в молекуле, увеличивается и массовая доля углерода, что приводит к повышению температуры плавления и кипения алкенов.
| Число углеродных атомов (n) | Формула | Массовая доля углерода |
|---|---|---|
| 2 | C2H4 | 0.6667 |
| 3 | C3H6 | 0.75 |
| 4 | C4H8 | 0.8 |
| 5 | C5H10 | 0.8333 |
Таким образом, массовая доля углерода в алкенах остается одинаковой из-за структурных особенностей этих органических соединений. Это имеет важное значение при определении и классификации алкенов и их химических и физических свойств.



