Ионная связь является одним из самых основных и фундаментальных типов химической связи, которая происходит между атомами, в результате чего образуются ионы. Она имеет огромное значение для понимания многих явлений и процессов в химии и физике, а также для разработки новых материалов и технологий.
Понимание ионной связи связано с представлениями о природе вещества. Уже в античности философы предполагали, что все вещества состоят из частиц – атомов. Но только в конце XIX века были сделаны научные открытия, которые позволили начать раскрытие тайн ионной связи.
Согласно современным представлениям, понятие ионной связи основывается на электростатическом притяжении между положительно и отрицательно заряженными ионами. Электроны, находящиеся на внешнем энергетическом уровне атомов, участвуют в образовании стабильных соединений путем передачи или разделения электронов.
Ионная связь: представления о природе
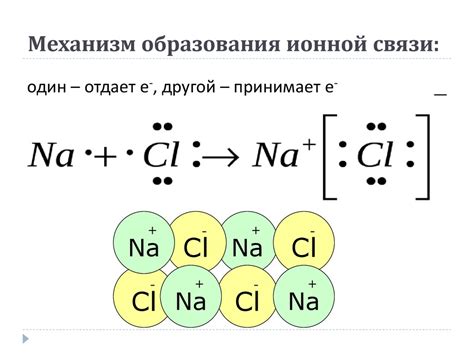
Атом состоит из ядра и электронной оболочки, в которой находятся электроны. Ядро атома содержит положительно заряженные протоны и нейтроны без заряда. Взаимодействие положительно заряженного ядра и отрицательно заряженных электронов образует электронную оболочку атома.
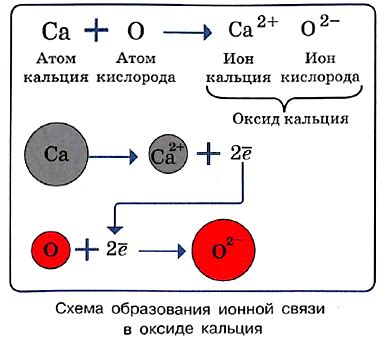
В процессе образования ионной связи происходит переход электронов от одного атома к другому. Некоторые атомы имеют повышенную электроотрицательность, что означает, что они сильнее притягивают электроны к себе. Такие атомы становятся отрицательно заряженными и называются анионами.
Другие атомы, которые отдают свои электроны, становятся положительно заряженными и называются катионами. Ионная связь возникает за счет притяжения между положительными и отрицательными зарядами. Это притяжение обуславливает прочность и стабильность ионных соединений.
Важно отметить, что ионная связь не является совершенно жесткой и нерушимой. Под воздействием других физических или химических факторов, ионная связь может слабеть или разрушаться. Также, ионная связь обладает определенными свойствами, которые существенно влияют на химические реакции, свойства веществ и их физическое состояние.
Определение ионной связи
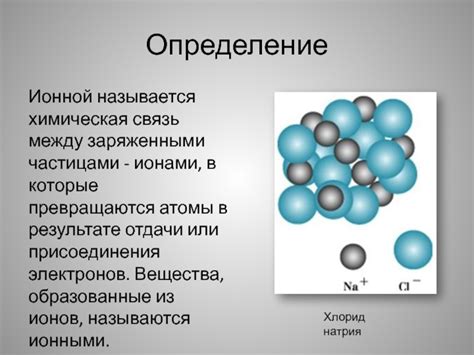
Основу ионной связи составляют электроны и ионы. Электроны, находящиеся на внешних энергетических уровнях атома, могут быть либо отданы, либо приняты другими атомами. Атомы, которые отдают электроны, становятся положительно заряженными ионами, так как у них появляется недостаток электронов на внешнем энергетическом уровне. Атомы, которые принимают электроны, становятся отрицательно заряженными ионами, так как их внешний энергетический уровень заполняется дополнительными электронами от другого атома.
Ионная связь образуется между атомами, которые сильно различаются по электроотрицательности. Такие атомы могут обменять электроны друг с другом, чтобы достичь более стабильного состояния. Если разница в электроотрицательности атомов не очень большая, образуется ковалентная связь. В случае ионной связи разница в электроотрицательности атомов значительно больше, и электроны полностью передаются от одного атома к другому.
Ионная связь играет важную роль в химии и имеет множество практических применений. Она присуща большому количеству соединений, включая соли и мины. Ионные связи влияют на физические и химические свойства веществ, такие как точка плавления, теплопроводность и растворимость. Понимание природы ионной связи позволяет ученым предсказывать и объяснять поведение соединений и создавать новые материалы с определенными свойствами.
Электростатические взаимодействия

В случае ионной связи, электростатическое взаимодействие происходит между ионами разных зарядов. Положительные ионы (катионы) притягивают отрицательные ионы (анионы), образуя кристаллическую решетку. Это происходит из-за разности сил притяжения и отталкивания между зарядами.
Ионная связь объясняется электростатическими взаимодействиями между ионами вещества. Ионы в ионной связи образуются, когда атомы теряют или получают электроны, образуя заряды, которые притягиваются друг к другу.
Рассмотрение электростатических взаимодействий позволяет более полно и систематически понять, как образуются ионные связи и какие свойства ионных соединений определяются этими взаимодействиями. Использование представлений о природе электростатических сил открывает двери к пониманию многих явлений в физике и химии.
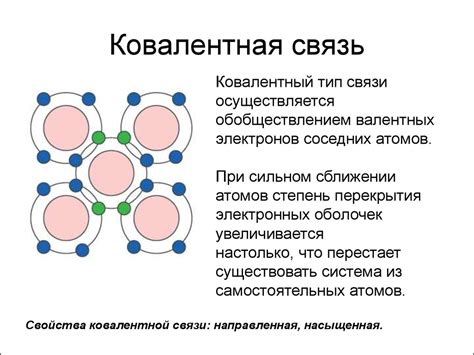
Модель кристаллической решетки
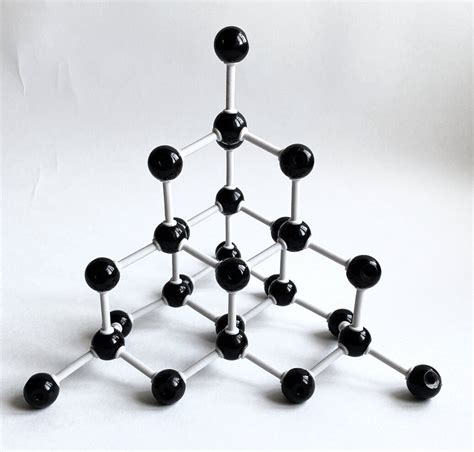
В кристаллической решетке положительно и отрицательно заряженные ионы взаимодействуют друг с другом благодаря притяжению противоположных зарядов. Модель кристаллической решетки помогает понять, как происходит образование ионных связей и почему ионы образуют устойчивые структуры.
Кристаллическая решетка может быть представлена как трехмерная сетка, в которой каждый узел представляет собой ион. Ионы различаются по заряду, поэтому положительно заряженные ионы располагаются рядом с отрицательно заряженными ионами, чтобы компенсировать заряды и достичь электронной нейтральности кристалла.
Модель кристаллической решетки помогает объяснить некоторые свойства ионных соединений, такие как высокая температура плавления и твердость. Также эта модель объясняет, почему ионные соединения проводят электрический ток только в расплавленном или растворенном состоянии, но не в твердом состоянии.
Идеальные и реальные ионы

Идеальные ионы - это абстрактные модели, которые представляют собой заряженные частицы в идеальном состоянии. Создание идеальных ионов позволяет упростить описание ионной связи и облегчить понимание ее основных принципов.
Реальные ионы представляют собой ионы, существующие в реальных условиях, с учетом всех факторов, таких как взаимодействие с другими частицами и растворителем. Реальные ионы могут иметь некоторые отличия от идеальных ионов, которые описываются с помощью идеализированных моделей.
Представления о природе ионы взаимодействия между идеальными и реальными ионами помогают нам понять, как образуются ионные соединения и как сильными могут быть ионные связи. Они также позволяют нам предсказывать свойства ионных соединений и объяснять их реакционную активность.
Идеальные и реальные ионы играют важную роль в наших представлениях о природе, помогая нам лучше понять и объяснить различные явления, связанные с ионными связями.
Поляризация ионов
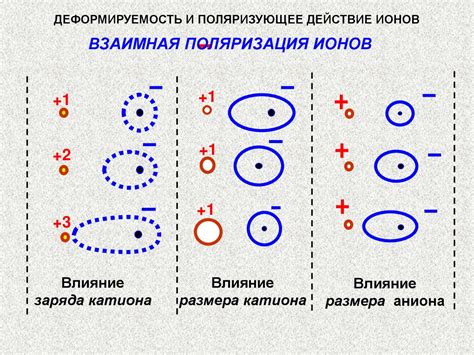
В ионной связи один ион приобретает отрицательный заряд, а другой - положительный. Ионы с противоположными зарядами притягиваются друг к другу и образуют стабильное соединение. Однако между ионами действуют электрические силы отталкивания, связанные с одноименными зарядами. Поскольку эти отталкивающие силы превалируют над притягивающими, вопрос заключается в том, как ионы все же связываются и образуют кристаллическую решетку.
Поляризация ионов фундаментальным образом влияет на образование ионной связи. В процессе связывания ионов их электронные оболочки подвергаются изменению. У иона с более высокой электроотрицательностью образуется отрицательный частичный заряд, тогда как у иона с более низкой электроотрицательностью возникает положительный частичный заряд. Такая поляризация ионов позволяет компенсировать отталкивающие силы и обеспечивает притяжение между ними.
Кроме того, поляризация ионов также определяет ряд других свойств ионной связи. Например, она влияет на поведение ионов в растворах, на температурные и механические свойства ионных кристаллов. От электронной поляризации зависит растворимость соединений и их способность реагировать с другими веществами.
Исследование поляризации ионов позволяет глубже понять природу ионной связи и причины ее образования. Это явление отображает сложность взаимодействия между частицами и подчеркивает роль электронной плотности в химических реакциях и связях между веществами.
Образование решетки ионной связи
Решетка ионной связи образуется в результате взаимодействия положительно и отрицательно заряженных ионов. Этот процесс происходит в результате электростатического притяжения между ионами разных зарядов.
Положительные ионы, такие как катионы металлов, стремятся отдать свои электроны и образовать ионы положительной заряды. Отрицательные ионы, как анионы неметаллов, получают электроны и образуют ионы отрицательной заряды. Эти два вида ионов притягиваются друг к другу и образуют решетку ионной связи.
Решетка ионной связи имеет регулярную структуру и состоит из положительных и отрицательных ионов, расположенных в определенном порядке. Каждый положительный ион окружен отрицательными ионами, и каждый отрицательный ион окружен положительными ионами. Это обеспечивает стабильность решетки ионной связи и делает ее прочной и устойчивой.
Образование решетки ионной связи происходит при образовании соединений, таких как соли. В этих соединениях положительные ионы металлов образуют решетку, а отрицательные ионы неметаллов занимают места в этой решетке. Решетка ионной связи обеспечивает стабильность и прочность солей и позволяет им образовывать кристаллы с определенной формой и структурой.
Образование решетки ионной связи является основой многих химических реакций и процессов. Ионные связи присутствуют во многих соединениях, таких как соли, оксиды и гидроксиды. Они играют важную роль в формировании химических соединений и их свойств, а также во многих естественных и промышленных процессах.
Свойства и качества ионной связи

Одним из главных свойств ионной связи является ее прочность. Ионная связь достаточно крепка и требует большого количества энергии для разрыва. Это обусловлено тем, что образование ионной связи сопровождается образованием электростатического поля вокруг каждого иона, которое оказывает силу притяжения на противоположно заряженные ионы. Эта сила притяжения является результатом действия электростатических сил, которые образуются из-за разности зарядов ионов.
Другим важным качеством ионной связи является ее направленность. Ионы образуют особый регулярный и упорядоченный кристаллический решетчатый строение, в котором каждый ион окружен несколькими ионами противоположного заряда. Это обеспечивает свойство ионной связи быть направленной и ориентированной в пространстве, что предполагает, что каждый ион обладает определенным координационным окружением и образует определенное число связей с соседними ионами.
Еще одним из важных свойств ионной связи является ее неполярность. Ижоль того, что ионы имеют неполные электронные оболочки, что делает ионные связи полярными по природе, при образовании ионной решетки такая полярность компенсируется, и в результате весь кристалл становится неполярным. Это свойство играет огромную роль во многих процессах и реакциях, связанных с ионной связью.
Также стоит отметить, что ионная связь обладает высокой точностью и регулярностью в своей структуре. Это свойство позволяет ионам занимать свои определенные позиции в кристаллической структуре, что является основой для образования кристаллов различных солей и минералов.
В целом, свойства и качества ионной связи объясняются представлениями о природе иона и его взаимодействии с другими ионами. Эти свойства делают ионную связь одной из наиболее важных форм химической связи и основу для формирования различных веществ и соединений.
Влияние внешних факторов на ионную связь

Ионная связь, как межатомное взаимодействие, может быть влияна различными внешними факторами, которые могут изменить ее силу и стабильность.
Один из таких факторов - это природа ионов, образующих связь. Заряд ионов, их размер и электроотрицательность влияют на силу ионной связи. Чем больше заряд ионов, тем сильнее будет ионная связь, так как кулоновское притяжение между ними будет сильнее. Кроме того, чем меньше размер ионов, тем ближе будут они друг к другу, что также усиливает ионную связь. Электроотрицательность ионов также влияет на силу связи - чем больше разница в электроотрицательности, тем сильнее будет ионная связь.
Температура является еще одним фактором, влияющим на ионную связь. При повышении температуры кинетическая энергия частиц увеличивается, что может привести к разрыву ионной связи. Поэтому температура может влиять на стабильность связи. Например, водный раствор соли может разлагаться при нагревании и терять свойство проводить электрический ток.
Другим важным фактором является растворитель, в котором находятся ионы. Растворитель может влиять на стабильность ионной связи и реакцию ионов. Вода, например, может разбавить ионы и разрушить связь, или наоборот, образовать гидратированные ионы и укрепить ионную связь.
Также, внешние силы, такие как давление и механическое воздействие, могут влиять на ионную связь. Увеличение давления может сжать ионы ближе друг к другу, что усилит ионную связь. Механическое воздействие, такое как деформация кристаллической решетки, может также влиять на стабильность связи.
Все эти внешние факторы могут взаимодействовать и оказывать влияние на ионную связь, изменяя ее силу и стабильность.
Применение ионной связи в технологии и науке
Ионная связь играет важную роль во многих областях технологии и науки. Ее уникальные свойства позволяют использовать ее в различных приложениях, начиная от химической промышленности и заканчивая разработкой новых материалов и лекарств.
Одним из применений ионной связи является производство электролитов для аккумуляторных батарей. Электролиты, содержащие ионы, обеспечивают передачу заряда между электродами и замыкают цепь внутри батареи. Ионная связь также используется в процессе электролиза при производстве металлов, как, например, алюминия.
Благодаря своей способности образовывать кристаллическую структуру, ионная связь также находит свое применение в создании материалов с определенными механическими и электронными свойствами. Например, керамика, содержащая ионные связи, обладает высокой твердостью, жаростойкостью и проводимостью тепла. Эти свойства делают ее идеальным материалом для изготовления посуды, плазменных панелей и других изделий, работающих в экстремальных условиях.
Ионная связь также играет важную роль в биохимии и фармакологии. Многие лекарственные препараты основаны на взаимодействии ионных связей с биологическими молекулами, такими как белки и нуклеиновые кислоты. Это позволяет селективно воздействовать на различные процессы в организме и использовать ионную связь для достижения конкретного эффекта.



