Постоянный состав веществ - это основа для понимания множества процессов, происходящих в химии и физике. Понимание причин и молекулярного строения вещества помогает установить его свойства, реактивность и возможные взаимодействия с другими веществами.
Одной из причин постоянного состава вещества является строение его молекул. Молекула - это наименьшая единица вещества, сохраняющая его свойства. Каждая молекула состоит из атомов, которые соединяются друг с другом по определенным правилам.
Молекулярное строение вещества определяется химическим составом, то есть теми элементами, из которых оно состоит, а также способом, которым эти элементы соединены между собой. Например, молекула воды состоит из двух атомов водорода и одного атома кислорода, которые соединены между собой ковалентными связями.
Состав веществ: основные компоненты и их роли
Одним из основных компонентов вещества являются элементы, которые состоят из атомов. Атомы различных элементов имеют разное количество протонов, нейтронов и электронов. В зависимости от количества этих элементов вещество может вести себя по-разному и иметь различные свойства.
Кроме элементов, вещества также могут содержать различные органические и неорганические соединения. Органические соединения состоят из углерода, водорода, а также других элементов, таких как кислород, азот, фосфор и другие. Неорганические соединения могут быть мелкими молекулами или полимерами и могут включать в себя такие вещества, как соли, оксиды и кислоты.
Каждый компонент вещества играет свою роль и влияет на его свойства и поведение. Например, элементы могут образовывать соединения, которые характеризуются определенным цветом, запахом или вкусом. Органические соединения могут быть основой для построения больших молекул, таких как белки, углеводы и липиды, которые являются основными компонентами живых организмов.
Важно понимать, что состав вещества может быть разнообразным и зависеть от его происхождения и природы. Изучение состава вещества позволяет нам лучше понять его свойства и использовать его в различных процессах и технологиях.
Причины наличия постоянного состава вещества

Во-первых, каждый химический элемент имеет свой уникальный атомный номер, определяющий количество протонов в ядре атома. Это число остается неизменным для данного элемента и обуславливает его химические свойства. В результате, любое соединение, содержащее данный элемент, будет иметь постоянное содержание данного атома в своем составе.
Во-вторых, молекулярное строение вещества также играет решающую роль в его составе. Молекулы вещества образуются за счет химических связей между атомами различных элементов. При образовании молекулы, атомы соединяются в определенном порядке и с определенным количеством. Поэтому, при нарушении или изменении молекулярной структуры, состав вещества может измениться.
Также, химические связи между атомами в молекулах являются крайне стабильными и требуют большого количества энергии для их разрыва. В результате, вещества могут сохранять свою химическую структуру при участии в различных химических реакциях.
Таким образом, постоянный состав вещества обусловлен комбинацией физических и химических факторов, таких как атомный номер элементов, молекулярное строение и стабильность химических связей. Знание этих факторов позволяет предсказывать состав вещества и строить соответствующие химические реакции и процессы.
Молекулярное строение и его влияние на свойства вещества
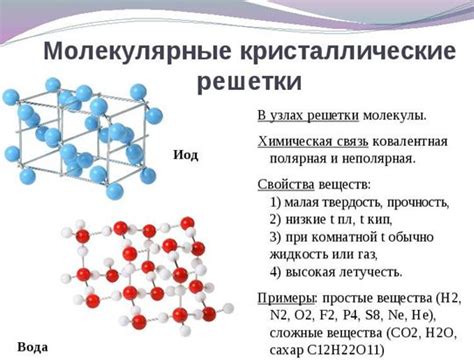
Одной из важных характеристик молекулярного строения вещества является его форма. Вещества с разными формами молекул могут иметь различные свойства. Например, молекулы сферической формы могут легко двигаться и смешиваться с другими веществами, в то время как молекулы полигональной формы могут образовывать кристаллическую структуру и обладать повышенной твердостью.
Другим важным аспектом молекулярного строения является его реакционная активность. Молекулы с определенной структурой могут иметь большую или меньшую способность вступать в химические реакции. Например, молекулы с двойной связью могут быть более реакционноспособными, чем молекулы с одинарной связью.
Также молекулярное строение может определять физические свойства вещества, такие как температура плавления и кипения, плотность, растворимость и др. Например, молекулы симметричной структуры обычно имеют более высокую точку плавления, чем молекулы несимметричной структуры.
Кроме того, молекулярное строение может влиять на электрические и оптические свойства вещества. Например, молекулярные кристаллы с определенной структурой могут обладать способностью проводить электрический ток или изменять показатели преломления света.
Исследование молекулярного строения вещества позволяет понять причины его свойств и использовать эту информацию для создания новых материалов с желаемыми характеристиками. Понимание взаимосвязи молекулярного строения и свойств вещества является важным фундаментом для развития науки, технологии и промышленности.
- Молекулярное строение определяет форму вещества
- Молекулярная форма влияет на физические и химические свойства
- Структура молекулы определяет реакционную активность
- Молекулярное строение влияет на температуру плавления и кипения
- Молекулярная структура может влиять на электрические и оптические свойства
Классификация состава вещества: органические и неорганические соединения

Вещества можно классифицировать по своему химическому составу. Существуют два основных типа веществ: органические и неорганические соединения.
Органические соединения состоят из атомов углерода, образующих основу их молекулярной структуры. Углерод является уникальным элементом, способным образовывать длинные цепи и кольца с другими атомами, такими как водород, кислород, азот и другие. Органические соединения широко распространены в природе и включают в себя такие вещества, как углеводы, жиры, белки и нуклеиновые кислоты.
Неорганические соединения включают в себя все остальные вещества, не содержащие углеродных атомов. Это могут быть различные металлы и их соединения, кислоты, основания, соли и прочие неорганические вещества. Неорганические соединения также имеют широкое применение в различных отраслях науки и промышленности.
Классификация веществ на органические и неорганические помогает упорядочить и систематизировать знания о составе и свойствах различных веществ. Органическая химия изучает органические соединения и их реакции, в то время как неорганическая химия занимается изучением неорганических соединений.
Изменение состава вещества: физические и химические процессы
Вещество может изменять свой состав под воздействием различных физических и химических процессов. Физические процессы характеризуются изменениями физических свойств вещества, сохраняя его химический состав. Такие процессы включают в себя изменение агрегатного состояния вещества (такие как плавление, кипение, сублимация), изменение формы и объема, разделение на фракции и т.д.
С другой стороны, химические процессы связаны с образованием новых веществ и изменением химического состава и структуры исходного вещества. В процессе химических реакций происходит разрыв связей между атомами и образование новых связей, что приводит к образованию новых соединений. Примерами химических процессов являются горение, окисление, гидролиз, ферментация и т.д.
Важно отметить, что физические и химические процессы могут происходить одновременно или последовательно, взаимодействуя друг с другом. Например, при нагревании вещества может происходить его плавление (физический процесс) и дальнейшее окисление (химический процесс).
Знание о изменении состава вещества и понимание физических и химических процессов являются фундаментальными для многих научных дисциплин, таких как физика, химия, биология и других. Понимание этих процессов также позволяет нам использовать и контролировать вещества в нашей повседневной жизни, например, при приготовлении пищи, производстве лекарств, в технологических процессах и во многих других областях.



