Валентность - это понятие в химии, которое указывает, сколько других атомов может связаться с данным атомом. Это своего рода "вместимость" атома. Валентность может быть положительной или отрицательной величиной, в зависимости от того, способен ли атом сформировать положительный или отрицательный ион.
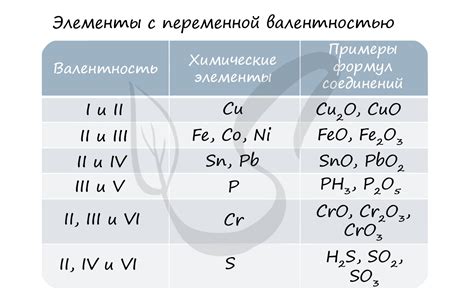
Однако существуют исключения, которые немного усложняют понимание валентности. Некоторые атомы могут иметь несколько вариантов валентности, что означает, что они могут образовывать различные типы химических связей с другими атомами. Например, металлы часто имеют несколько вариантов валентности, что позволяет им образовывать разные ионы и химические соединения.
Одним из примеров таких атомов является железо. Валентность железа может варьироваться от +2 до +6. В состоянии +2, железо может образовывать соединения, в которых два электрона передаются другому атому. В состоянии +6, железо может образовывать соединения, в которых шесть электронов передаются другому атому.
Что такое валентность
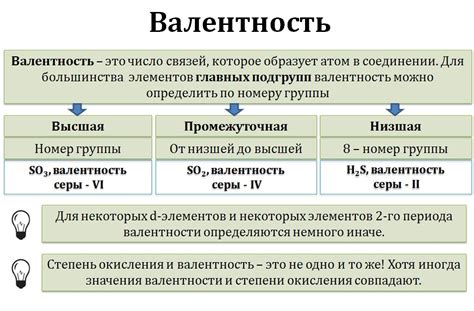
Валентность может быть положительной, отрицательной или нейтральной. Положительная валентность означает, что частица может образовывать связи с другими частицами и при этом теряет электроны. Отрицательная валентность указывает на способность частицы принимать электроны, образуя связи с другими частицами. Нейтральная валентность означает, что частица не образует связей и не теряет или не принимает электроны.
Валентность может быть выражена числом или знаком. Числовая валентность указывает на количество электронов, которые могут быть переданы или приняты в процессе образования связей. Знаковая валентность показывает, какой тип ионов может образовать частица - положительные или отрицательные.
Некоторые частицы имеют постоянную валентность, например, металлы обычно имеют положительную валентность, а неметаллы - отрицательную. Однако существуют и исключения, когда валентность может быть разной в разных соединениях.
Валентность играет ключевую роль в понимании химических реакций и образования химических связей между атомами. Она помогает предсказывать свойства и состав химических соединений и способность веществ взаимодействовать друг с другом.
Определение валентности
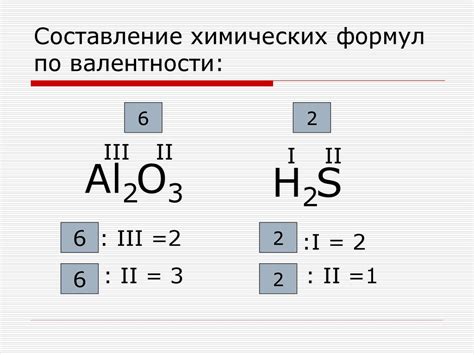
Как правило, валентность атома равна числу электронов, которые он может отдать или принять. Например, атом кислорода имеет валентность 2, потому что он может принять два электрона, чтобы достичь восьмиэлектронной оболочки, а атом натрия имеет валентность 1, потому что он может отдать один электрон.
Однако существуют исключения из этого правила. Некоторые элементы имеют переменную валентность, что означает, что они могут образовывать связи с разным количеством электронов. Например, железо может иметь валентность 2 или 3, а серебро - 1 или 2.
Также следует отметить, что валентность может быть положительной или отрицательной. Атомы с положительной валентностью отдают электроны, а атомы с отрицательной валентностью принимают электроны. Это является основой образования ионов и образования химических соединений.
Валентность играет важную роль в понимании структуры и свойств химических соединений. Она позволяет определить тип связей между атомами и предсказать реакционную способность вещества. Изучение валентности помогает химикам разрабатывать новые соединения и оптимизировать их свойства для различных применений.
Как измерить валентность
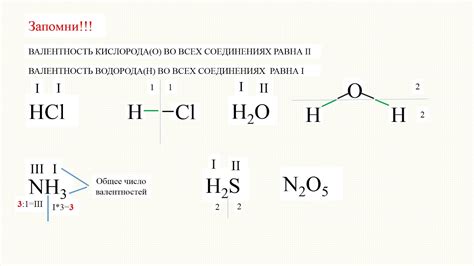
Один из распространенных методов измерения валентности - использование лексико-семантических баз данных. Эти базы данных содержат большое количество слов и выражений, снабженных различными значениями и оценками валентности. С помощью таких баз данных можно определить валентность отдельных слов и выражений и использовать эти данные для анализа текстов.
Другой метод измерения валентности - создание специализированных корпусов текстов. В таких корпусах тексты размечаются с помощью аннотаторов, которые оценивают валентность отдельных слов и фраз. Затем проводится статистический анализ полученных данных, что позволяет определить среднюю валентность для различных типов текстов или конкретных слов.
Также существуют методы измерения валентности с использованием машинного обучения. На основе размеченных данных, модель обучается определять валентность текстового материала. Эти методы позволяют автоматизировать процесс измерения валентности и обрабатывать большие объемы текста.
Однако стоит отметить, что измерение валентности является сложной задачей, которая не всегда может быть решена полностью автоматически. В некоторых случаях оценка валентности требует контекстного анализа и понимания семантической структуры текста.
В целом, современные методы измерения валентности позволяют получить информацию о настроении, оценке и эмоциональной окраске текстового материала. Эта информация может быть полезна в различных областях, таких как анализ социальных медиа, маркетинговые исследования, анализ общественного мнения и другие.
Типы валентности
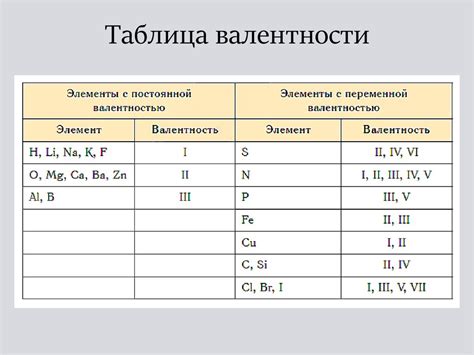
У слов и глаголов может быть различное число валентных позиций. Существуют следующие типы валентности:
1. Одно- или моновалентные слова и глаголы: это слова, которые могут связываться только с одним аргументом. Например, глагол "дышать" требует только одного аргумента - "воздух".
2. Двух- или дивалентные слова и глаголы: это слова, которые могут связываться с двумя аргументами. Например, глагол "дать" требует двух аргументов - "даритель" и "получатель".
3. Трех- или тривалентные слова и глаголы: это слова, которые могут связываться с тремя аргументами. Например, глагол "показать" требует трех аргументов - "субъекта", "объекта" и "адресата".
4. Многовалентные слова и глаголы: это слова, которые могут связываться с более чем тремя аргументами. Например, глагол "разделить" может иметь множество аргументов - "донора", "результат", "получатель" и т.д.
Некоторые слова и глаголы могут иметь разную валентность в разных контекстах. Например, глагол "стоять" может быть моновалентным, если он используется без дополнения ("стоял"), и дивалентным, если он используется с дополнением ("стоял под деревом").
Таким образом, понимание и определение типов валентности важно для понимания синтаксических конструкций и грамматической структуры предложения.
Примеры высокой валентности
- Глаголы с высокой валентностью:
- Любить - можно любить кого-то, что-то или делать что-то с любовью.
- Готовить - можно готовить еду, готовить людей к чему-то или готовиться к чему-то.
- Учить - можно учить кого-то, что-то или учиться чему-то.
- Предлоги с высокой валентностью:
- С - можно с кем-то говорить, ходить, работать или сделать что-то с кем-то.
- По - можно поехать, поговорить, пообедать или почитать что-то.
- За - можно забрать, заплатить, заботиться или захватить что-то.
- Существительные с высокой валентностью:
- Друг - можно иметь друга, быть другом или делать что-то для друга.
- Дом - можно построить, купить, снять или жить в доме.
- Работа - можно искать работу, иметь работу, делать работу или говорить о работе.
Это лишь небольшой пример слов с высокой валентностью. В русском языке есть много других слов, которые могут сочетаться с различными конструкциями и образовывать разнообразные предложения.
Примеры низкой валентности
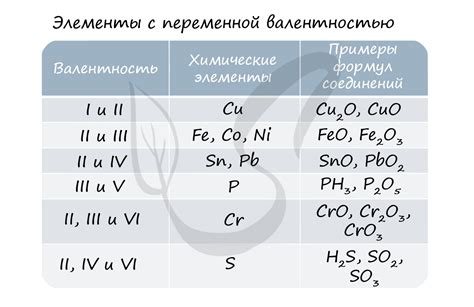
Низкая валентность встречается у некоторых элементов и соединений, где атомы обладают небольшим количеством связей. Это может быть вызвано различными причинами, такими как специфическая электронная конфигурация или особенности химической связи.
Один из примеров низкой валентности - бор. У атома бора всего три электрона во внешней оболочке, поэтому он может образовывать только три связи. В результате бор образует соединения с низкой валентностью, например, бораны.
| Соединение | Структура | Описание |
|---|---|---|
| Боран |  | Соединение бора и водорода. В нем бор образует три связи с водородом. |
| Димер борана |  | Две молекулы борана могут образовывать сложную структуру с низкой валентностью. |
Еще одним примером соединений с низкой валентностью являются бис(циклопентадиен) металлы. В этих соединениях у металла имеется низкая валентность, так как он образует две связи с двумя кольцами циклопентадиена.
| Соединение | Структура | Описание |
|---|---|---|
| Бис(циклопентадиен)никель |  | Соединение, в котором никель образует две связи с двумя кольцами циклопентадиена. |
| Бис(циклопентадиен)железо |  | Соединение, в котором железо образует две связи с двумя кольцами циклопентадиена. |
Эти примеры показывают, что низкая валентность может проявляться у различных элементов и соединений, что делает их особенными и интересными для изучения.
Примеры исключений в валентности
Прилагательное "одетый" примерно соответствует глаголу "одеть". Обычно глагол "одеть" имеет два аргумента: того, кто одевает, и того, кого одевают. Но прилагательное "одетый" не требует второго аргумента. Например, в предложении "Мальчик одет" глагол "одет" не имеет аргумента, т.е. его валентность равна нулю.
Еще одним примером исключения в валентности может служить глагол "спать". Обычно глагол "спать" имеет один аргумент - подлежащее, которое спит. Однако, существует выражение "сонный идти", где глагол "спать" используется без аргумента. В этом случае его валентность также равна нулю.
Еще одним интересным примером является глагол "прощать". Обычно глагол "прощать" имеет два аргумента: того, кто прощает, и того, кого прощают. Однако есть выражение "быть прощенным", где глагол "прощать" используется без аргументов. В этом случае его валентность также равна нулю.
Такие исключения в валентности могут быть интересными для лингвистического анализа и могут указывать на особенности языка и его эволюцию в процессе времени.
Влияние валентности на химические реакции
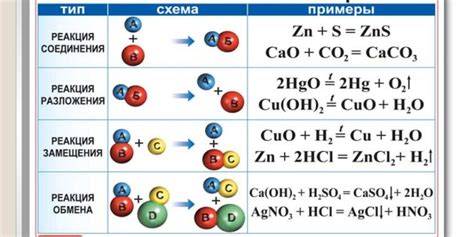
Валентность играет важную роль в химических реакциях, определяя ориентацию и скорость протекания реакций. Она позволяет определить, какие атомы могут образовать химическую связь и в каком количестве, а также какие ионы могут образовываться в результате реакции.
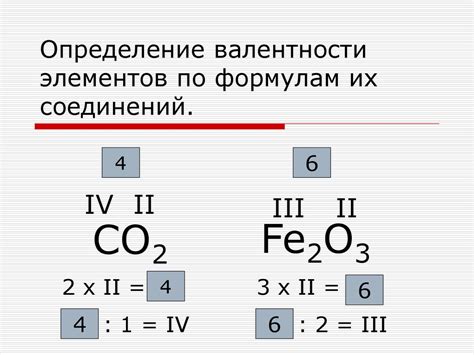
Валентность атома определяется количеством свободных электронов в его внешней электронной оболочке. Чем больше свободных электронов, тем больше атом способен образовывать связей с другими атомами. Например, углеродный атом имеет четыре свободных электрона, поэтому его валентность равна 4.
Валентность атомов определяет химическую формулу соединения и количество атомов каждого элемента в нём. Например, вода (H2O) состоит из двух атомов водорода и одного атома кислорода. Валентность кислорода равна 2, а валентность водорода - 1. Используя эти значения, можно определить, какие элементы могут образовывать связи и в каком количестве.
| Валентность | Примерные значения |
|---|---|
| 1 | водород (H), натрий (Na) |
| 2 | кислород (O), кальций (Ca) |
| 3 | азот (N), алюминий (Al) |
| 4 | углерод (C), кремний (Si) |
В химических реакциях валентность атомов может меняться, что приводит к образованию новых соединений и изменению свойств исходных веществ. Например, при горении метана (CH4) валентность углерода изменяется с 4 до 2, а валентность кислорода увеличивается с 2 до 4. В результате образуется два новых соединения - карбоновый оксид (CO) и вода (H2O).
Таким образом, понимание валентности атомов позволяет предсказывать и объяснять химические реакции, а также синтезировать новые соединения с определенными свойствами. Изучение валентности является одним из важных аспектов химической науки.
Валентность в органической химии

Валентность в органической химии определяет количество связей, которые элемент может образовать или принять в химической реакции.
Органические соединения состоят из углеродных атомов, которые образуют объединения с другими атомами, такими как водород, кислород, азот и другие элементы. Каждый углеродный атом может формировать четыре связи, что обуславливает его валентность 4.
Однако существуют исключения, где валентность углерода может быть отличной от 4. Например, во времена Нвайенго (XIX век) было сформулировано правило пенталентности углерода, которое объясняло его способность образовывать пять связей. Это правило было опровергнуто в дальнейшем, однако существует некоторое количество органических соединений, таких как гиперкоординированные арены и син 107, которые образуют пятую связь с углеродом.
Также стоит отметить, что валентность элемента может зависеть от его окружения и условий реакций. Например, во многих случаях атом кислорода образует две связи, и его валентность составляет 2. Однако, в реакциях с различными элементами или соединениями, кислород может образовывать более двух связей и иметь валентность больше 2.
Важно помнить, что валентность - это концептуальный инструмент, используемый для облегчения понимания структуры и свойств органических соединений, но не всегда строго соответствует реальным значениям связей и электронного распределения в молекулах.
Значение валентности в медицине
Когда речь идет о валентности атомов, в медицине наибольшую важность приобретает валентность кислорода. Валентность кислорода позволяет ему образовывать связи с другими атомами и образовывать структуру молекулы. Так, например, кислород может образовывать связи с водородом, образуя молекулу воды. Это важно для понимания таких физиологических процессов, как дыхание и образование энергии в организме.
Кроме этого, валентность играет роль и в понимании взаимодействия препаратов с биологическими молекулами. Например, если препарат обладает определенной валентностью, он может присоединяться к рецепторам на клеточной поверхности, вызывая определенный фармакологический эффект. Такие препараты могут быть использованы в лечении различных заболеваний, таких как рак или инфекции.
Валентность также важна при изучении взаимодействия вирусов с клетками человека. Вирусы обладают определенной валентностью, которая позволяет им присоединяться к рецепторам на клеточной поверхности и проникать внутрь клетки. Понимание валентности вирусов помогает разрабатывать противовирусные препараты, которые могут блокировать взаимодействие вируса с клеткой и предотвращать развитие заболевания.



