Лед является одним из самых известных и удивительных веществ в природе. Он обладает уникальными физическими свойствами, и одно из них - его способность таять. В холодной воде лед образует кристаллы, которые медленно растворяются в окружающей среде. Однако, при добавлении соли в воду, процесс таяния льда ускоряется необычным образом.
Физическое явление таяния льда под воздействием соли давно привлекает внимание ученых. Известно, что соль в воде образует раствор, который имеет более низкую температуру замерзания, чем чистая вода. Это означает, что при добавлении соли, температура окружающей воды может быть значительно ниже нуля градусов Цельсия, что приводит к более быстрому таянию льда.
Существует научное объяснение этого явления. Когда соль попадает на поверхность льда, она образует пленку, состоящую из молекул соли и воды. Эта пленка вызывает ускоренное таяние льда, так как солевая вода имеет нижнюю точку замерзания. Молекулы соли проникают во внутреннюю структуру льда, снижая его плотность и вызывая таяние.
Интересно, что этот процесс таяния льда под воздействием соли используется в обычной жизни, например, для очистки дорог от льда и снега. Соль, рассыпанная на ледяной поверхности, способствует его быстрому таянию и обеспечивает безопасность движения транспорта.
Физическое явление таяния льда

При нормальных условиях вода замораживается при температуре 0°C. Это происходит благодаря формированию упорядоченной структуры кристаллической решетки льда, в которой каждая молекула воды тесно связана с соседними молекулами. Однако, в наличии соли в воде можно наблюдать таяние льда при температурах ниже 0°C.
Ключевой механизм этого явления заключается в том, что соль обладает свойством понижать точку замерзания воды. Это связано с тем, что соль вступает в реакцию с молекулами воды, образуя ионы и мешая образованию кристаллической решетки льда. Когда вода содержит достаточно соли, температура, при которой происходит таяние льда, может быть существенно ниже нуля градусов Цельсия.
Таяние льда под воздействием соли играет важную роль в различных областях нашей жизни. Это используется в технологиях оттаивания льда на дорогах и тротуарах, в обработке и хранении пищевых продуктов, а также в промышленных процессах, требующих контроля и управления температурой.
Исследование физического явления таяния льда под воздействием соли помогает нам лучше понять основные принципы взаимодействия молекул и развить новые технологии, воздействующие на состояние льда в нашей жизни.
Влияние соли на таяние льда

Осмос - это процесс перемещения частиц раствора через полупроницаемую мембрану с меньшей концентрацией к раствору с большей концентрацией. В случае с таянием льда, соль действует как мембрана, разделительная лед от воды.
Когда соль добавляется к льду, она начинает взаимодействовать с молекулами воды во льду, вызывая их распад и образование ионов. Эти ионы мигрируют к поверхности льда, где они создаются.
Так как соль разделяет воду и лед, она позволяет воде таять при более низких температурах, чем обычно. Это явление известно как замерзание точки плавления или снижение температуры замерзания.
Важно отметить, что количество добавленной соли влияет на скорость таяния льда. Чем больше соли добавлено, тем быстрее он начнет таять.
Влияние соли на таяние льда имеет практическое применение. Например, в холодильной промышленности соль используется для быстрого замораживания пищевых продуктов или создания льда в ледогенераторах. Также соль используется для устранения льда и снега с дорог при низких температурах.
Различие между таянием льда с солью и без нее

Основное различие заключается в температуре таяния льда с солью и без нее. Обычно, вода замерзает при 0 градусах Цельсия и тает при этой же температуре. Однако, при добавлении соли, точка замерзания воды снижается, а точка таяния повышается до отрицательных значений.
При соприкосновении с солью, лед начинает таять быстрее, так как соль обладает свойством понижать температуру замерзания воды. Механизм заключается в том, что соль разлагается на ионы в растворе, а ионы проникают в лед и мешают молекулам воды собираться в кристаллическую решетку. Это позволяет воде находиться в жидком состоянии при температуре ниже 0 градусов Цельсия.
Таким образом, соль способствует уменьшению температуры замерзания воды и повышению ее температуры таяния. Этот эффект широко используется для решения различных задач, таких как соление дорог зимой, консервация пищевых продуктов и даже приготовление мороженого.
Механизм взаимодействия соли с льдом

Основная причина, почему соль способствует таянию льда, заключается в изменении точки замерзания воды под воздействием солей. Обычная точка замерзания чистой воды составляет 0 градусов по Цельсию. Однако, когда вода содержит растворенные соли, ее точка замерзания снижается. Это происходит потому, что соли взаимодействуют с молекулами воды, препятствуя им собираться в кристаллической решетке льда.
Взаимодействие соли с льдом происходит посредством процесса диффузии. Когда соль попадает на поверхность льда, ее молекулы перемещаются по концентрационному градиенту к месту, где соли меньше. Диффузия солей происходит внутри льда, в том числе между его кристаллическими структурами.
В результате, соль и вода образуют раствор, который является источником тепла. При образовании раствора происходит выделение теплоты, что приводит к повышению температуры льда и его последующему таянию. Таким образом, взаимодействие соли с льдом приводит к его быстрому таянию и образованию жидкой воды.
| Процесс | Описание |
|---|---|
| Проникновение соли в структуру льда | Соль проникает внутрь льда и взаимодействует с молекулами воды |
| Изменение точки замерзания | Соли снижают точку замерзания воды, препятствуя образованию льда |
| Диффузия солей внутри льда | Молекулы солей перемещаются по концентрационному градиенту, включая внутри льда |
| Образование раствора | Соль и вода образуют раствор, который выделяет тепло и приводит к таянию льда |
Расщепление ионов при растворении соли в воде
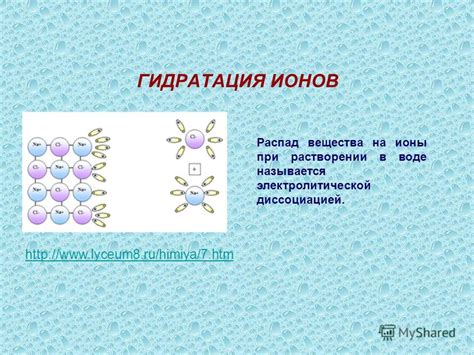
Расщепление ионов происходит из-за взаимодействия соли с молекулами воды. В процессе растворения соль разделяется на положительно заряженные ионы катионы) и отрицательно заряженные ионы (анионы). Например, при растворении хлорида натрия (NaCl) образуются ионы натрия (Na+) и ионы хлорида (Cl-).
Расщепление ионов полностью зависит от типа соли, ее концентрации в растворе и температуры. Этот процесс происходит благодаря силам, которые существуют между ионы в растворе и водными молекулами. В результате взаимодействия соли с водой происходит разрушение электростатических связей между атомами и образуются новые электростатические связи между ионами и молекулами воды.
Расщепление ионов при растворении солей играет важную роль в понимании явления таяния льда под воздействием соли. Наличие ионов в водной среде изменяет свойства воды, позволяя ей оставаться в жидком состоянии при очень низких температурах и кристаллизоваться при таянии льда.
| Ион | Заряд |
|---|---|
| Na+ | Положительный |
| Cl- | Отрицательный |
Процесс диффузии соли через лед
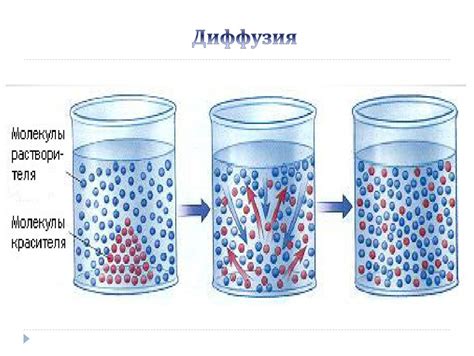
Соленая вода имеет ниже температуру замерзания, чем чистая вода. Под воздействием соли лед начинает таять. Этот процесс объясняется явлением диффузии.
Диффузия - это самопроизвольное перемешивание молекул одного вещества с молекулами другого вещества в результате их случайных тепловых движений. При контакте с льдом, молекулы соли начинают диффундировать - двигаться от более высокой концентрации (соленой воды) к более низкой концентрации (ледяной поверхности).
Процесс диффузии соли через лед происходит благодаря различию в концентрации соли в соленой воде и льду. Молекулы соли имеют меньшую массу и меньший размер, поэтому они могут проникать сквозь кристаллическую структуру льда. Затем они перемещаются по воде в диффузионной зоне между льдом и соленой водой.
В результате диффузии соли через лед происходит потеря молекул льда, что приводит к его таянию. Чем больше соль содержится в воде, тем выше концентрация соли в диффузионной зоне и тем быстрее происходит процесс таяния льда.
Изучение процесса диффузии соли через лед позволяет лучше понять физическую природу явления и разработать методы его контроля и использования в различных областях, таких как пищевая промышленность и окружающая среда.



