Мир вокруг нас населен различными веществами, которые состоят из молекул – мельчайших частиц, образующих все вещества вокруг. При изучении молекул мы можем наблюдать интересное явление – притяжение между ними.
Данное явление объясняется наличием физико-химических сил, таких как ван-дер-ваальсовы силы и электромагнитное притяжение. Однако, несмотря на наличие этих сил, мы не можем не заметить промежутки между молекулами.
Почему же так происходит? Ответ заключается в структуре и форме молекул. Молекулы могут иметь различные формы и размеры, что приводит к разным расстояниям между ними. Кроме того, некоторые молекулы могут находиться на расстоянии друг от друга из-за наличия свободных пространств.
Почему между молекулами есть промежутки?

Молекулы состоят из атомов, которые состоят из ядра и электронных оболочек. Почти весь объем атома занимают электронные оболочки, которые содержат электроны, находящиеся на различных орбиталях. Под действием сил электростатического притяжения электроны находятся в постоянном движении вокруг ядра и образуют области, где вероятность обнаружить электрон высока.
Взаимодействие между молекулами происходит посредством электростатических сил. Притяжение положительно заряженных ядер одной молекулы к отрицательно заряженным электронам другой молекулы создает силы притяжения между ними. Однако эти силы притяжения настолько слабы, что не могут полностью устранить промежутки между молекулами.
Кроме того, взаимодействие между молекулами ослабляется их движением. Молекулы находятся в постоянном движении и сталкиваются друг с другом. При столкновении молекулы отскакивают друг от друга, создавая промежутки между ними.
Таким образом, причина появления промежутков между молекулами связана с особенностями строения и движения молекул, а также с силами взаимодействия между ними. Эти промежутки играют важную роль в таких процессах, как фазовые переходы, диффузия и реакции, и влияют на свойства вещества.
Молекулы и их взаимодействие

Взаимодействие между молекулами играет важную роль в химии и физике. Оно определяет физические и химические свойства вещества, такие как температура плавления и кипения, плотность, вязкость и т.д. Взаимодействие между молекулами можно разделить на два основных типа: притяжение и отталкивание.
Притяжение между молекулами происходит благодаря силам ван-дер-Ваальса, диполь-дипольным взаимодействиям и водородным связям. Силы ван-дер-Ваальса - это слабые притяжения между электрическими диполями, образовавшимися временно внутри молекулы. Диполь-дипольные взаимодействия возникают между молекулами, имеющими постоянные диполи. Водородные связи - это особый тип диполь-дипольного взаимодействия, где водородный атом участвует в связи с более электроотрицательным атомом.
Отталкивание между молекулами происходит из-за электрического отталкивания между зарядами электронов. Когда молекулы находятся на достаточно близком расстоянии друг от друга, заряды электронов начинают отталкиваться, создавая отрицательное электрическое давление.
Промежутки между молекулами объясняются комбинацией притяжения и отталкивания. Силы притяжения притягивают молекулы друг к другу, но отталкивание между электронами создает промежутки между ними. Эти промежутки важны для определения объема и формы вещества, а также для его физических и химических свойств.
В целом, взаимодействие между молекулами является сложным и многообразным процессом, и его изучение позволяет лучше понять строение и свойства вещества.
Физические свойства молекул

Одно из основных физических свойств молекул - их притяжение друг к другу. Это происходит благодаря силам взаимодействия, которые возникают на межмолекулярном уровне.
Притяжение между молекулами может быть слабым или сильным, в зависимости от химической природы вещества. Оно происходит благодаря электромагнитным силам и влияет на множество физических свойств, таких как температура плавления и кипения, плотность, вязкость и т. д.
Промежутки между молекулами возникают из-за отталкивающих сил между ними. Молекулы обладают некоторым размером и формой, и поэтому их расположение в пространстве ограничено. Это приводит к тому, что между молекулами образуются свободные области, промежутки, которые могут быть заполнены другими молекулами или частицами.
Промежутки между молекулами имеют важное значение для физических процессов, таких как диффузия и реакции. Они позволяют молекулам перемещаться свободно и взаимодействовать друг с другом.
Понимание физических свойств молекул и их взаимодействия имеет большое значение в химии, физике и других научных областях. Изучение этих свойств позволяет лучше понять структуру вещества и его поведение в различных условиях.
Термодинамическое равновесие
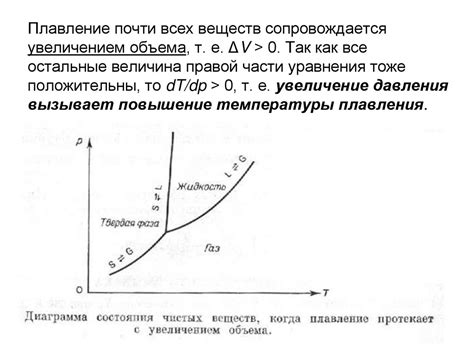
Молекулы, находящиеся в притяжении друг к другу, стремятся достичь термодинамического равновесия. Термодинамическое равновесие означает, что система находится в состоянии, в котором нет никаких изменений или перемещений молекул.
Промежутки между молекулами в притяжении обусловлены движением молекул, их тепловым движением. Каждая молекула постоянно движется, сталкиваясь и взаимодействуя с другими молекулами. Это движение создает промежутки между молекулами, так как они не могут быть непосредственно в контакте друг с другом.
В результате теплового движения и взаимодействия молекул, система стабилизируется в состоянии, при котором количество молекул, находящихся в определенном расстоянии друг от друга, находится в равновесии. Молекулы стремятся к минимальной энергии и стабильному распределению в пространстве.
Эти промежутки между молекулами в притяжении также обусловлены силами отталкивания между молекулами, которые действуют на близких расстояниях. Эти силы препятствуют молекулам приближаться друг к другу слишком близко, и заставляют их оставаться на определенном расстоянии друг от друга.
Таким образом, промежутки между молекулами в притяжении обусловлены как тепловым движением молекул, так и силами отталкивания между ними. Эти факторы вместе обеспечивают термодинамическое равновесие системы и определяют структуру и свойства вещества.
Основные принципы молекулярной взаимодействия

Одной из причин присутствия промежутков между молекулами является отталкивание электронных облаков. Вещества состоят из атомов, в которых находятся электроны, вращающиеся по определенным орбитам. Электроны находятся в электронных облаках, которые занимают определенный объем. Когда два атома или молекулы приближаются друг к другу, электронные облака начинают отталкиваться, из-за чего образуются промежутки между молекулами.
Кроме того, молекулы могут притягиваться друг к другу благодаря взаимодействию ионных или дипольных моментов. В ионных взаимодействиях заряженные атомы или молекулы притягиваются друг к другу в результате образования ионных связей. В дипольных взаимодействиях заряженные и полярные области молекул притягиваются друг к другу, образуя дипольные связи. Эти два типа межмолекулярных взаимодействий также могут приводить к образованию промежутков между молекулами.
Промежутки между молекулами также могут быть обусловлены энергетическими и энтропийными эффектами. В некоторых случаях, молекулы могут предпочитать занимать определенные позиции в пространстве, чтобы минимизировать энергию системы. Это может приводить к образованию промежутков между молекулами. Также, молекулы имеют тенденцию к перемещению в более хаотические состояния для увеличения энтропии системы, что также может вызывать образование промежутков.
| Принципы молекулярной взаимодействия: | Описание: |
|---|---|
| Электростатические силы | Притяжение и отталкивание заряженных и поляризованных частиц |
| Отталкивание электронных облаков | Образование промежутков из-за отталкивания электронных облаков |
| Ионные и дипольные взаимодействия | Притяжение заряженных и полярных областей между молекулами |
| Энергетические и энтропийные эффекты | Минимизация энергии и увеличение энтропии системы |
Межмолекулярные силы
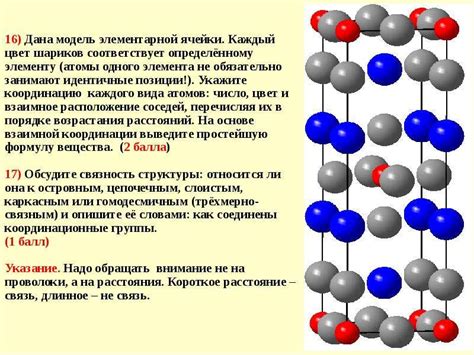
Однако, несмотря на наличие таких сил, существуют промежутки между молекулами. Это связано с тем, что межмолекулярные силы имеют ограниченную дальность действия и убывают с расстоянием.
Промежутки между молекулами являются результатом баланса межмолекулярных сил притяжения и теплового движения молекул. В силу теплового движения молекулы постоянно изменяют свои положения, создавая хаотическое распределение, которое обуславливает промежутки между ними.
Эти промежутки между молекулами могут быть различной величины, в зависимости от типа вещества и его физических свойств. Например, в газах промежутки между молекулами сравнительно большие, что объясняет их высокую подвижность и способность распространяться во всех направлениях.
В жидкостях промежутки между молекулами уже меньше, что придает им свойства текучести и сжимаемости. В твердых веществах промежутки между молекулами наименьшие, что обуславливает их строение и упругость.
Таким образом, промежутки между молекулами существуют в силу совместного действия межмолекулярных сил притяжения и теплового движения молекул. Они играют важную роль в объяснении свойств и поведения вещества в природе.
Роль промежутков между молекулами
Промежутки между молекулами играют важную роль в притяжении и взаимодействии между ними. Эти промежутки возникают из-за отталкивания электронных облаков, которые окружают атомы молекул.
Когда молекулы находятся на расстоянии друг от друга, электронные облака создают зоны повышенной и пониженной плотности электронов. В зоне повышенной плотности электронов существует электростатическое отрицательное поле, в то время как в зоне пониженной плотности электронов это поле положительное. Эти поля притягивают между собой молекулы и создают межмолекулярное взаимодействие.
Промежутки между молекулами также влияют на физические свойства веществ, такие как точка плавления и кипения, плотность, вязкость и т. д. Когда молекулы находятся близко друг к другу, их взаимодействие усиливается, что приводит к повышению точки плавления, увеличению плотности и вязкости. Наоборот, когда промежутки между молекулами увеличиваются, их взаимодействие ослабевает, что может привести к снижению точки плавления, плотности и вязкости.
Знание роли промежутков между молекулами является важным для понимания многих физических и химических процессов, таких как фазовые переходы и дисперсные силы. Это позволяет ученым разрабатывать новые материалы с определенными свойствами и улучшать существующие.
Влияние промежутков на свойства вещества
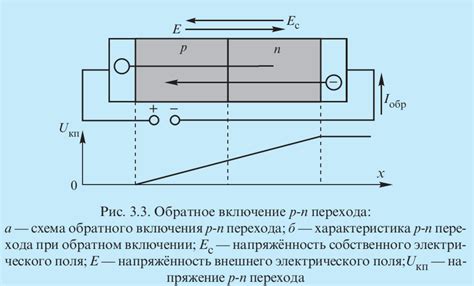
Промежутки между молекулами вещества играют важную роль в его свойствах. Эти промежутки могут повлиять на такие характеристики, как плотность, теплопроводность, растворимость и температура плавления вещества.
Промежутки между молекулами являются результатом слабых сил межмолекулярного взаимодействия, таких как ван-дер-ваальсовы силы, диполь-дипольное взаимодействие и водородная связь. Хотя эти силы слабы по сравнению с химическими связями внутри молекулы, они все же оказывают значительное влияние на свойства вещества.
Промежутки между молекулами влияют на плотность вещества. Чем больше промежутки, тем меньше плотность вещества, так как в большом объеме присутствует меньшее количество молекул. Например, газы имеют очень большие промежутки между молекулами, поэтому они обладают низкой плотностью. В то время как твердые вещества имеют малые промежутки между молекулами, что придает им высокую плотность.
Также промежутки между молекулами влияют на теплопроводность вещества. Чем больше промежуток, тем хуже вещество проводит тепло. Это связано с тем, что передача тепла осуществляется через столкновение частиц друг с другом. Если промежутки между частицами большие, тепло будет передаваться медленнее.
Растворимость вещества также зависит от промежутков между молекулами. Чем больше промежутки, тем лучше вещество растворяется. Промежутки позволяют растворителю проникать между молекулами и разделить их. Например, соль, которая имеет малые промежутки между молекулами, лучше растворяется в воде, которая имеет большие промежутки.
Наконец, промежутки между молекулами влияют на температуру плавления вещества. Чем больше промежуток, тем ниже температура плавления вещества. Это связано с тем, что для плавления вещества требуется преодолеть силы притяжения между молекулами. Если промежутки между молекулами большие, эти силы будут слабее и вещество будет плавиться при более низкой температуре.
Таким образом, промежутки между молекулами играют важную роль в определении свойств вещества. Понимание этих промежутков позволяет более глубоко изучить характеристики различных веществ и их поведение в различных условиях.
Применение знания о промежутках между молекулами
Одним из применений данного знания является разработка новых материалов с определенными свойствами. Загазованная жидкость, например, может быть использована в производстве твердых пенопластовых материалов, таких как полистирол. Знание о промежутках между молекулами позволяет контролировать плотность материала и его теплопроводность.
Другим применением является разработка новых лекарственных препаратов. Многие лекарства имеют специфическую структуру молекулы, и знание об интермолекулярных промежутках позволяет ученым точно определить их физические и химические свойства. Это позволяет проводить более точные исследования о влиянии лекарственных препаратов на организм.
Также, знание об интермолекулярных промежутках используется в различных областях материаловедения и электроники. Ученые разрабатывают новые материалы, которые обладают предпочтительными электронными и физическими свойствами. Нанотехнологии, например, основаны на понимании и контроле интермолекулярных промежутков, и позволяют создавать микросхемы и устройства малых размеров с повышенной производительностью.
Наконец, знание о промежутках между молекулами также применяется в космической инженерии и аэрокосмической технике. При разработке материалов и конструкций для космических аппаратов необходимо учитывать экстремальные условия, такие как высокая или низкая температура, вакуум и радиационное излучение. Знание интермолекулярных промежутков помогает создавать материалы, которые могут выдерживать такие условия без потери своих свойств.
| Знание о промежутках между молекулами позволяет: |
|---|
| Разрабатывать новые материалы и продукты. |
| Улучшать технологии и разрабатывать новые лекарственные препараты. |
| Разрабатывать материалы и конструкции для космической инженерии. |
Перспективы исследования промежутков между молекулами

Одна из перспектив исследования промежутков между молекулами заключается в применении этих знаний в различных областях науки и технологий. Например, понимание промежутков между молекулами может привести к созданию более эффективных материалов с улучшенными свойствами, такими как прочность, устойчивость к разрыву и теплоизоляционные характеристики. Это может быть полезно в разработке новых материалов для применения в авиационной, космической и автомобильной промышленности.
Исследования промежутков между молекулами также могут привести к разработке новых лекарственных средств. Понимание взаимодействия молекул в организме может помочь ученым создать более эффективные и безопасные препараты для лечения различных заболеваний.
Кроме того, исследование промежутков между молекулами имеет важное значение для понимания глобальных проблем, таких как изменение климата. Влияние промежутков на взаимодействие молекул в атмосфере может помочь ученым предсказать и моделировать изменения погоды и климата, что может привести к разработке новых методов и стратегий для уменьшения воздействия на окружающую среду.
Таким образом, исследование промежутков между молекулами представляет собой актуальную и перспективную область научных исследований, которая имеет потенциал для принесения значительных научных и практических результатов в различных областях. Повышение наших знаний в этой области может привести к созданию новых материалов, лекарств и технологий, способных преобразовать нашу жизнь и улучшить качество обитания на Земле.



