Кальцинированная сода, также известная как натриевая соль, является одним из наиболее широко используемых химических веществ в мире. Она имеет множество применений в промышленности, кулинарии, медицине и многих других отраслях. Однако, несмотря на ее многочисленные полезные свойства, кальцинированная сода имеет один интересный аспект - она не растворима в воде.
Растворимость - это способность вещества растворяться в данной жидкости при определенных условиях. В большинстве случаев, с особыми исключениями, солями натрия, такими как кальцинированная сода, атомы натрия и гидроксида (ОН) вступают в химическую реакцию с водой, образуя ионные связи и образуя хидроксионные (OH-) и гидроксидные (Na+) ионы.
Однако, кальцинированная сода - это исключение из этого правила. При добавлении кальцинированной соды в воду, требуется существенное количество энергии, чтобы нарушить связи и проникнуть в молекульную структуру соли. В результате получается, что частицы кальцинированной соды остаются нерастворимыми и плавают в воде в виде осадка.
Что такое кальцинированная сода?

Кальцинированная сода обладает рядом уникальных свойств, которые делают ее полезной в различных областях промышленности и быта. Она обладает щелочными свойствами и широко применяется в производстве стекла, моющих средств, косметики и пищевой промышленности. Кроме того, кальцинированная сода находит применение в медицине, а также в процессе очистки воды и удаления загрязнений.
Отличительной чертой кальцинированной соды является ее нерастворимость в воде. В отличие от обычной соды, которая легко растворяется при взаимодействии с водой, кальцинированная сода имеет низкую скорость растворения и не диссоциирует полностью. Ее нерастворимость обусловлена изменением структуры молекулы при нагревании, в результате чего она становится менее реакционноспособной и не способна образовывать ионы, необходимые для растворения в воде.
Таким образом, кальцинированная сода играет важную роль в различных областях науки и промышленности благодаря своим уникальным свойствам, которые определяются ее структурой и нерастворимостью в воде.
Состав кальцинированной соды

Состав кальцинированной соды состоит из главных компонентов:
- Натрия (Na) - основная химическая составляющая кальцинированной соды. Она является основным реагентом при ее производстве и обладает щелочными свойствами.
- Углерода (C) - другой ключевой элемент кальцинированной соды. Он придает соединению его кристаллическую структуру и помогает определить его химические свойства.
- Кальция (Ca) - кальцинированная сода содержит небольшое количество кальция, который может присутствовать в виде примеси. Кальций имеет важное значение для многих биологических процессов и может влиять на некоторые свойства соединения.
Кальцинированная сода обладает низкой растворимостью в воде, что делает ее полезной в ряде применений, таких как производство стекла, моющие средства и прочие промышленные процессы. Этот субстанция имеет широкий спектр применений благодаря своим химическим свойствам и стабильному составу.
Процесс получения кальцинированной соды
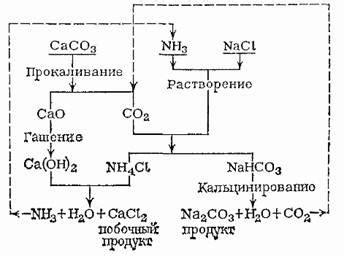
Процесс получения кальцинированной соды начинается с нагревания обычной пищевой соды до температуры около 850 градусов Цельсия. При этой высокой температуре молекулы соды теряют молекулярную воду и претерпевают декомпозицию.
Реакция превращает обычную пищевую соду в кальцинированную соду и выделяет два побочных продукта - воду и углекислый газ (CO2). Полученная кальцинированная сода (Na2CO3) имеет белый кристаллический вид и является щелочным соединением с широким спектром применения. Она используется в производстве стекла, мыла, моющих средств, жидкостей для обработки бумаги и многих других отраслях промышленности.
Помимо этого, кальцинированная сода также применяется в процессе очистки воды и на фармацевтических предприятиях. Она часто используется в необработанной форме или используется для производства других химических соединений, таких как сода пепельная (Na2CO3·H2O).
Свойства кальцинированной соды

Одно из самых важных свойств кальцинированной соды - это ее устойчивость к растворению в воде. Обычная сода (NaHCO3) хорошо растворима в воде и образует щелочной раствор. Однако кальцинированная сода не растворяется в воде и не образует щелочной раствор. Это связано с изменением структуры молекулы NaHCO3 при кальцинировании. В результате обработки при высокой температуре, гидроксильные группы (OH) в структуре молекулы превращаются в окисное гидроксильные группы (O), что делает соду не растворимой в воде.
Кальцинированная сода также обладает щелочными свойствами, так же как и обычная сода. Она может взаимодействовать с кислотными соединениями, образуя соли и выделяя углекислый газ (CO2). Такая реакция называется нейтрализацией и используется, например, в кулинарии для разрыхления теста.
Однако стоит отметить, что кальцинированная сода не является безопасным веществом для употребления в пищу, так как оксид кальция, образующийся при ее кальцинировании, может вызывать различные проблемы со здоровьем при проникновении в организм, поэтому ее использование ограничено и не рекомендуется в кулинарии или других областях, связанных с употреблением в пищу.
| Свойство | Описание |
|---|---|
| Растворимость в воде | Не растворима |
| Химическая формула | CaCO3 |
| Щелочные свойства | Да |
| Ограничения использования | Не рекомендуется употреблять в пищу |
Не растворимость в воде
Основное объяснение такой не растворимости кальцинированной соды связано с тем, что при нагревании происходит декарбоксилизация, то есть освобождение углекислого газа (CO2). В результате этого процесса образуется сода основного типа, которая обладает гидратационными свойствами, но уже не растворима в воде.
Не растворимость кальцинированной соды в воде также связывают с ее кристаллической структурой. При нагревании и декарбоксилизации сода теряет свою решетку и превращается в аморфный порошок, что делает ее нерастворимой в воде. Кристаллическая структура обычной соды способствует ее растворимости в воде, тогда как кальцинированная сода теряет это свойство.
Таким образом, кальцинированная сода, хотя и имеет химическую формулу NaHCO3, отличается своими физическими и химическими свойствами от обычной соды. Ее не растворимость в воде объясняется декарбоксилизацией и изменением структуры, что делает ее более подходящей для определенных процессов, таких как использование в качестве агента поглощения кислорода или для удаления нежелательных запахов.
Высокая температура плавления
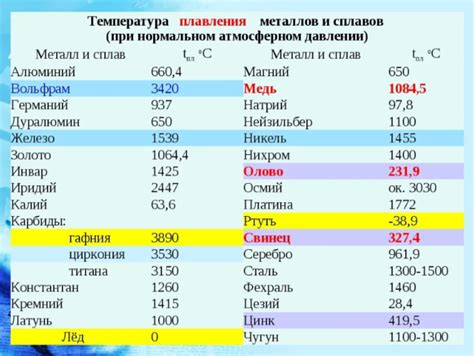
Высокая температура обжига (около 850 градусов Цельсия) приводит к тому, что молекулы кальцинированной соды становятся очень стабильными и твердыми. Это объясняет ее нерастворимость в обычной воде. Большинство веществ растворяются в воде благодаря слабым химическим связям, которые легко прерываются при контакте с молекулами воды. Однако кальцинированная сода обладает очень прочными связями и, следовательно, не распадается при взаимодействии с водой.
Причины не растворимости кальцинированной соды в воде

1. Ионная связь: Кальцинированная сода образует кристаллы, в которых ионы натрия и гидроксида связаны между собой сильными ионными связями. Эти связи сопротивляются разрушению в воде, что делает растворение этого вещества очень медленным и неполным.
2. Малейший коэффициент растворимости: Концентрация растворенных ионов гидроксида натрия в кальцинированной соде очень низкая. Это связано с тем, что молекулы гидроксида натрия слабо разрушаются в воде, а извлечение этих ионов из кристаллической решетки оказывается затруднительным.
3. Рестрикция твердых растворов: Вода, будучи жидкостью, обладает определенной ограниченной способностью растворять твердые вещества. Скорость растворения и количество растворенного вещества ограничиваются числом доступных растворимых мест в воде. Если эти места заполнены другими веществами, растворение кальцинированной соды замедляется или становится невозможным.
В итоге, несмотря на возможность некоторого растворения кальцинированной соды в воде, его количественное значение является настолько низким, что в реакциях и процессах, требующих высокой подвижности ионов, это вещество обычно считается не растворимым.
Сложная структура кристаллической решетки
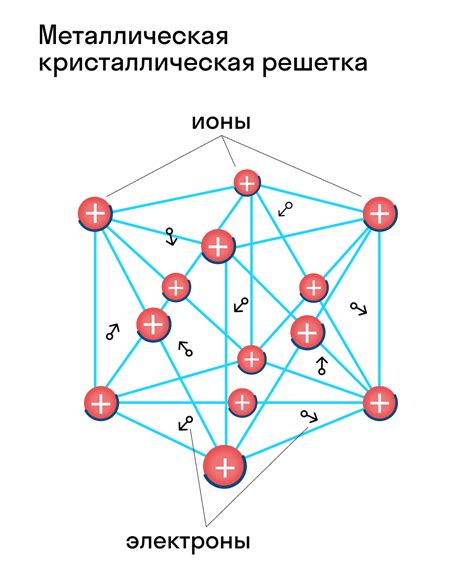
Кальцинированная сода оказывается не растворимой в воде из-за ее сложной кристаллической структуры. Кристаллическая решетка соды содержит анионы карбоната (CO32-), которые упакованы внутри структуры кристалла, образуя гексагональные рельсы.
Эти рельсы растянуты и связаны друг с другом катионами кальция (Ca2+), которые находятся между анионами карбоната. Такая сложная структура решетки делает молекулы кальцинированной соды устойчивыми и позволяет им сохраняться в твердом состоянии.
При попытке растворить кальцинированную соду в воде, молекулы воды должны разрушить связи между анионами карбоната и катионами кальция, чтобы заместить катионы и достичь точки насыщения. Однако эти связи очень крепкие, и образование новых связей с водой является энергетически нефаворизированным процессом.
Таким образом, кристаллическая структура кальцинированной соды предотвращает ее растворение в воде, делая ее практически нерастворимой в обычных условиях.
| Анион | Катион |
|---|---|
| CO32- | Ca2+ |
Отсутствие электрического заряда

При кальцинировании соды происходит процесс нагревания, при котором карбонат натрия (Na2CO3) теряет воду. Это приводит к образованию оксида кальция (CaO), который уже не имеет способности образовывать ионы и растворяться в воде.
Таким образом, кальцинированная сода не обладает электролитичностью и не может образовывать раствор в воде, так как отсутствует необходимый электрический заряд для сопротивления электрическому полю воды.



