Плавление алюминия - это процесс, вызываемый повышением температуры для преодоления сил межатомного взаимодействия и изменения его состояния из твердого в жидкое. Однако, несмотря на то что плавление алюминия является физическим процессом, в процессе данного преобразования происходят и некоторые химические реакции, которые влияют на его свойства и состав.
Алюминий имеет очень высокую точку плавления - около 660 градусов по Цельсию. Это связано с его кристаллической структурой и энергией, необходимой для разрыва связей между атомами и преодоления сил притяжения. Когда алюминий нагревается до достаточно высокой температуры, его структура начинает распадаться, и атомы алюминия становятся подвижными, а также взаимодействуют с окружающей средой.
В ходе плавления алюминия происходит окисление поверхности металла. При контакте с воздухом, атомы алюминия соединяются с кислородом, образуя оксид натрия - тонкую пленку оксида на поверхности, которая защищает металл от дальнейшей реакции с окружающей средой. Окисление алюминия также влияет на его плавление, поскольку образовавшийся оксид изменяет температуру плавления металла и его термофизические свойства.
Таким образом, плавление алюминия - это комплексный процесс, включающий физические и химические аспекты. Физически, плавление алюминия связано с преодолением сил притяжения между атомами, что приводит к изменению его состояния. Однако, химическое взаимодействие с окружающей средой, особенно окисление поверхности металла, также играет важную роль в процессе плавления и свойствах получившейся жидкой фазы алюминия.
Плавление алюминия: физический процесс или химическая реакция?

Алюминий является металлом, который обладает относительно низкой температурой плавления - около 660 градусов Цельсия. При достижении этой температуры металл начинает плавиться и превращается в жидкую форму. Это происходит благодаря тому, что атомы алюминия начинают двигаться быстрее и меняют свою структуру, формируя движущуюся "решетку" алюминиевых ионов внутри жидкого металла.
Химическая реакция, с другой стороны, предполагает изменение химического состава вещества, образование новых химических связей и обмен энергией. Но при плавлении алюминия не происходят такие химические изменения. Алюминий остается алюминием, только его физическое состояние меняется.
Плавление алюминия имеет значительное применение в различных сферах, от производства алюминиевых изделий до использования в литейной промышленности. Возможность плавления алюминия позволяет его перерабатывать и использовать вновь, что делает его эффективным и экологически чистым материалом.
Физическое и химическое состояние алюминия

Физический вид алюминия при комнатной температуре и давлении - серебристо-белый металл, мягкий и легкий. Он обладает высокой теплопроводностью и отлично проводит электричество. При повышении температуры алюминий расширяется, а при охлаждении сжимается, что делает его очень подходящим для использования в различных отраслях промышленности, включая авиацию, производство автомобилей, строительство и упаковку.
Химический алюминий является достаточно активным элементом. Он реагирует с кислородом в воздухе и образует оксид алюминия (Al2O3), также известный как криолит. Данный оксид образует прочную пленку на поверхности алюминия, которая защищает его от дальнейшей коррозии.
Физические и химические свойства алюминия делают его очень востребованным материалом в промышленности. Его высокая теплопроводность, легкость и прочность делают его идеальным выбором для производства легкого оборудования и конструкций. Алюминий также используется в производстве различных емкостей, упаковки и бытовых предметов.
| Свойство | Значение |
|---|---|
| Атомный номер | 13 |
| Атомная масса | 26.98 г/моль |
| Температура плавления | 660.32°C |
| Температура кипения | 2467°C |
| Плотность | 2.70 г/см3 |
| Теплопроводность | 237 Вт/(м·К) |
| Электрическая проводимость | 37.7 м/Ом·мм² |
Физический процесс плавления
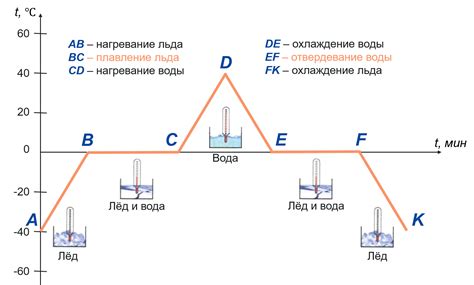
Когда алюминий плавится, его атомы не подвергаются химическому изменению – они лишь меняют физическое состояние. Физическое плавление характеризуется основными свойствами, такими как изменение формы вещества, его плотности и объема, при сохранении химического состава. При остывании расплавленного алюминия он вновь становится твердым и обретает свою кристаллическую структуру.
Таким образом, процесс плавления алюминия – это физическое явление, которое происходит благодаря изменению энергии межатомного взаимодействия, вытекающего из изменения температуры вещества.
Температура плавления алюминия
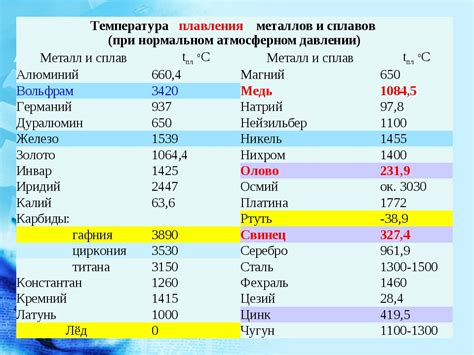
Температура плавления алюминия составляет около 660 градусов Цельсия (1220 градусов по Фаренгейту). Это относительно низкая температура, по сравнению с другими металлами, такими как медь или железо. Благодаря этому, алюминий может быть плавлен и формован при более низких температурах, что делает его легко обрабатываемым материалом.
Интересно отметить, что температура плавления алюминия более чем в два раза ниже его точки кипения, которая составляет около 2519 градусов Цельсия (4566 градусов по Фаренгейту). Такое различие связано с особенностями атомной структуры алюминия и влияет на его свойства при переходе из твердого состояния в жидкое.
Знание температуры плавления алюминия важно не только для производства металлических изделий, но также для расчетов при использовании алюминия в различных технических и инженерных решениях. Эта информация позволяет эффективно контролировать процесс плавления и избегать потери материала.
Физические изменения при плавлении

Во время плавления алюминия происходят ряд физических изменений. Во-первых, твердое вещество начинает нагреваться и его температура начинает повышаться. При достижении температуры плавления, которая составляет около 660 градусов по Цельсию, алюминий начинает плавиться.
Плавление алюминия сопровождается изменением его физических свойств. Одно из основных изменений – это изменение агрегатного состояния вещества. Твердое вещество превращается в жидкость, что обусловлено перемещениями атомов и молекул друг относительно друга.
Другим физическим изменением, которое происходит при плавлении алюминия, является увеличение объема вещества. Когда алюминий плавится, его объем увеличивается на приблизительно 6%. Это объясняется особенностями молекулярной структуры алюминия.
Плавление алюминия также сопровождается изменением физических свойств самой жидкости. Например, ее вязкость становится намного меньше, что позволяет алюминию свободно течь и формировать различные формы при охлаждении. Также, алюминий становится проводником электричества и тепла при плавлении.
Таким образом, плавление алюминия – это физический процесс, который сопровождается изменением агрегатного состояния вещества, увеличением объема, уменьшением вязкости и появлением электрических и тепловых проводников. Понимание этих физических изменений помогает нам лучше понять сам процесс плавления алюминия.
Химические изменения при плавлении

Причиной химических изменений при плавлении алюминия является изменение фазы вещества. На фазовом переходе с твердого состояния в жидкое, атомы алюминия приобретают большую подвижность. Это приводит к возможности реакций между алюминием и окружающими веществами, например, кислородом из воздуха.
В результате контакта расплавленного алюминия с воздухом происходит окисление. Атомы алюминия соединяются с молекулами кислорода, образуя оксид алюминия (Al2O3). Этот оксид образует пленку на поверхности алюминия, которая защищает его от дальнейшего окисления. Именно благодаря этой пленке алюминий обладает высокой стойкостью к коррозии и агрессивным воздействиям окружающей среды.
| Пример реакции при плавлении алюминия: |
|---|
| 4Al + 3O2 → 2Al2O3 |
Важно отметить, что при плавлении алюминия химические реакции с участием других веществ, таких как добавки или примеси, могут происходить на более высоких температурах. Например, добавка меди может вызывать окрашивание расплава в красный цвет при формировании сплава.
Таким образом, плавление алюминия является физическим процессом, сопровождающимся химическими изменениями, которые происходят в результате контакта расплавленного алюминия с воздухом или другими веществами.
Причины плавления алюминия

Плавление алюминия связано с его кристаллической структурой и особыми свойствами межатомных связей. В чистом виде алюминий образует кубическую сетку, где каждый атом окружен восемью ближайшими соседями.
Обеспечивая электрическую проводимость и теплопроводность, межатомные связи внутри кристаллической структуры алюминия являются слабыми. Кроме того, низкое энергетическое значение этих связей указывает на небольшое количество энергии, необходимое для разрыва атомных связей.
При нагревании алюминия энергия, передаваемая атомам материала, увеличивает их колебания и позволяет преодолеть силы притяжения между ними. Когда достигается температура плавления, энергия настолько увеличивается, что атомы разрушают свои связи и вещество переходит из твердого состояния в жидкое.
Таким образом, причина плавления алюминия заключается в низкой энергии межатомных связей и возможности передачи энергии от внешнего источника, такого как нагрев, для преодоления этих сил притяжения.
Объяснение процесса плавления

Плавление алюминия происходит по следующей схеме: при нагревании алюминий получает энергию в виде тепла, что приводит к возрастанию скорости движения атомов в его кристаллической структуре. При достижении определенной температуры кинетическая энергия атомов становится достаточно большой, чтобы преодолеть силы притяжения между ними и разрушить кристаллическую решетку, превращая алюминий в жидкость.
Важно отметить, что процесс плавления алюминия не сопровождается химическими реакциями или образованием новых веществ. Все изменения происходят на уровне атомов, при этом химический состав алюминия остается неизменным.
Таким образом, плавление алюминия является физическим процессом, вызванным нагреванием и нарушением кристаллической структуры металла, что приводит к изменению его агрегатного состояния с твердого на жидкое без образования новых веществ.



