Температура кипения – это температура, при которой жидкость переходит в газовое состояние. Однако, мало кто знает, что эта температура может изменяться в зависимости от внешних условий, в частности от давления. Давайте разберемся, почему это происходит и какие факторы влияют на температуру кипения.
Все вещества имеют определенную молекулярную структуру и взаимодействуют друг с другом. При повышении давления на вещество, межмолекулярные силы становятся более сильными, что приводит к увеличению энергии, необходимой для перехода жидкости в газообразное состояние. Таким образом, температура кипения увеличивается.
В то же время, снижение давления на вещество ослабляет межмолекулярные силы и уменьшает энергию, необходимую для перехода вещества из жидкого в газообразное состояние. В результате, температура кипения снижается.
Следует отметить, что изменение температуры кипения в зависимости от давления является характерной особенностью каждого вещества. Например, вода при нормальных условиях кипит при температуре 100 градусов Цельсия. Однако, при увеличении давления ее температура кипения может достигать значений выше 100 градусов. И наоборот, при снижении давления температура кипения воды может понижаться, даже до температуры ниже нуля градусов Цельсия, при условии, что давление достаточно низкое.
Таким образом, изменение температуры кипения в зависимости от внешнего давления является важной характеристикой вещества и играет важную роль во многих процессах, таких как кипение воды при приготовлении пищи, работа паровых двигателей и многое другое.
Изменение температуры кипения
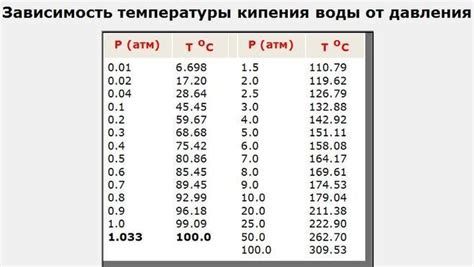
Увеличение давления приводит к повышению температуры кипения вещества. Это объясняется тем, что при повышенном давлении молекулы вещества более сильно притягиваются друг к другу и требуется больше энергии, чтобы перейти в газообразное состояние. Поэтому, чтобы вещество начало кипеть, необходимо повысить температуру.
Снижение давления, наоборот, вызывает понижение температуры кипения. При уменьшении внешнего давления молекулы вещества слабее притягиваются друг к другу и могут проще перейти в газообразное состояние. Поэтому, чтобы вещество начало кипеть, достаточно снизить температуру.
Изменение температуры кипения может быть использовано в различных процессах и технологиях. Например, в кипячении пищи при гораздо более низких температурах, чем обычно, можно использовать вакуумные устройства или устройства снижения давления. Также, изменение температуры кипения может быть полезно при кондиционировании воздуха, в процессе очистки и дистилляции воды и во многих других областях.
Таким образом, изменение температуры кипения в зависимости от внешнего давления – это важное явление, которое может быть использовано в различных технологических процессах и приложениях. Понимание этого явления позволяет разрабатывать новые методы и устройства, оптимизировать процессы и повышать эффективность многих технологий.
Как влияет внешнее давление на температуру кипения?

Это можно объяснить физико-химическими закономерностями. Когда давление увеличивается, парциальное давление молекул жидкости также увеличивается, что означает, что молекулы будут чаще выходить из жидкой фазы в газообразную. Это приводит к более высокой температуре кипения.
С другой стороны, с понижением внешнего давления парциальное давление молекул жидкости снижается, и молекулы более свободно переходят в газообразное состояние. В результате температура кипения уменьшается.
Таким образом, внешнее давление оказывает прямое влияние на температуру кипения. Это явление широко применимо в реальной жизни, например, при готовке пищи на больших высотах или при использовании давкокипящих котлов.
Важно отметить, что изменение внешнего давления также может повлиять на кипение другими способами. Например, высокое давление может создать более плотную структуру жидкости, что тоже может повысить температуру кипения. Однако, основное влияние осуществляется именно через изменение парциального давления.
Зависимость температуры кипения от давления
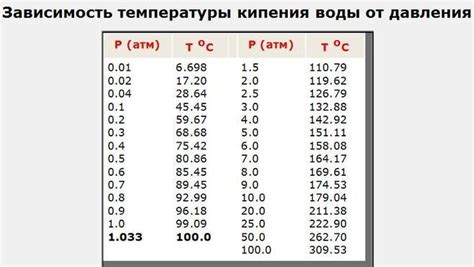
Согласно закону Рауля, открытому в 1887 году французским физиком и химиком Франсуа Мариусом Роланом Раулем, температура кипения жидкости зависит от внешнего давления. Закон Рауля устанавливает, что при повышении давления насыщенного пара вещества, его температура кипения также повышается и наоборот, при понижении давления температура кипения снижается.
Так, при увеличении внешнего давления насыщенного пара жидкости, молекулы пара подвергаются сильному сжатию, что приводит к их более частым столкновениям со своими соседними молекулами и повышению температуры кипения. Наоборот, при снижении давления насыщенного пара молекулы пара получают больше свободы и могут легче покинуть поверхность жидкости, что снижает температуру кипения.
Таким образом, внешнее давление является важным фактором, определяющим температуру кипения вещества. Понимание зависимости температуры кипения от давления позволяет ученным предсказывать и контролировать процессы испарения и конденсации, а также проводить эксперименты по изменению характеристик вещества при различных условиях.
Изменение температуры кипения в зависимости от внешнего давления
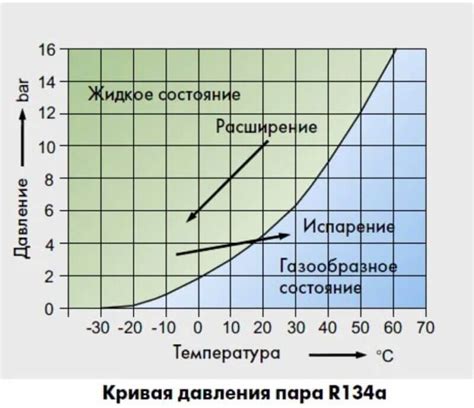
В обычных условиях при нормальном атмосферном давлении температура кипения воды составляет 100 градусов Цельсия. Однако если внешнее давление повышается или понижается, температура кипения также изменяется.
Повышение внешнего давления приводит к увеличению температуры кипения жидкости. Это связано с тем, что при повышенном давлении частицам жидкости требуется больше энергии для преодоления межмолекулярных сил и перехода в газообразное состояние. Поэтому температура кипения поднимается.
Снижение внешнего давления, наоборот, уменьшает температуру кипения жидкости. При пониженном давлении частицам жидкости требуется меньше энергии для перехода в газообразное состояние, поскольку межмолекулярные силы становятся менее значительными. Поэтому температура кипения опускается.
Знание об изменении температуры кипения в зависимости от внешнего давления имеет практическое значение в различных областях, таких как фармацевтическое и пищевое производство, химическая промышленность и многие другие. Это позволяет управлять процессами кипения, контролировать консистенцию и качество продуктов, а также разрабатывать новые технологии на основе этих закономерностей.
Как изменяется температура кипения при изменении давления?
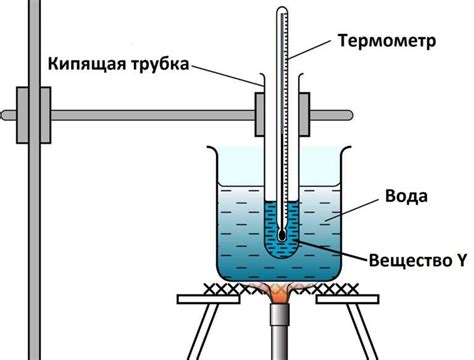
Температура кипения вещества зависит от давления, под которым происходит процесс кипения. При увеличении внешнего давления температура кипения повышается, а при уменьшении давления она снижается.
Это связано с тем, что при повышении давления увеличивается сила, с которой молекулы вещества удерживаются в жидком состоянии. В результате, для того чтобы перейти из жидкого состояния в газообразное, молекулам необходимо преодолеть большую силу притяжения. Поэтому, для начала превращения вещества в газообразное состояние, молекулам необходимо иметь большую энергию, что достигается повышением температуры.
С другой стороны, при уменьшении давления сила притяжения между молекулами уменьшается, что делает процесс перехода в газообразное состояние более легким. Следовательно, для перевода вещества из жидкого состояния в газообразное при низком давлении требуется меньшая температура.
Таким образом, изменение давления влияет на межмолекулярные силы и энергию молекул, что приводит к изменению температуры кипения вещества.
Влияние внешнего давления на точку кипения
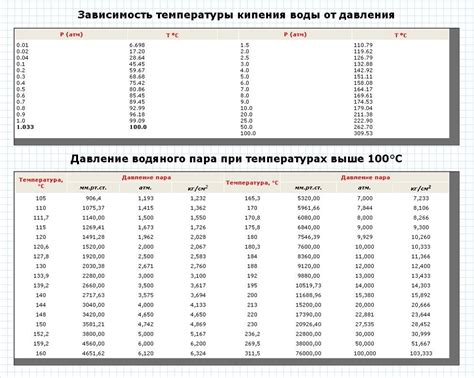
Температура кипения вещества зависит от внешнего давления. При увеличении давления точка кипения повышается, а при уменьшении давления точка кипения снижается.
Это явление объясняется законом Рауля. Согласно этому закону, при добавлении нерастворимого вещества в растворе, давление парового насыщения растворителя уменьшается пропорционально количеству добавленного вещества.
Когда внешнее давление повышается, то давление пара над жидкостью также возрастает. При этом молекулы жидкости сталкиваются с более высокими давлениями и чаще возвращаются в жидкое состояние, что препятствует образованию пара. Это приводит к повышению температуры, необходимой для достижения точки кипения.
Наоборот, при уменьшении внешнего давления, давление пара над жидкостью снижается. Молекулы жидкости сталкиваются с более низкими давлениями и реже возвращаются в жидкое состояние, что способствует образованию пара при более низкой температуре. Таким образом, точка кипения снижается.
Это явление можно наблюдать в реальной жизни. Например, в горах, на больших высотах, атмосферное давление ниже, что приводит к снижению точки кипения воды. В результате, вода начинает кипеть при более низкой температуре.
Знание о влиянии внешнего давления на точку кипения является важным в химии и на практике. Это позволяет контролировать температуру кипения при различных условиях, что полезно для проведения химических реакций и различных технологических процессов.
Почему температура кипения изменяется в зависимости от давления?
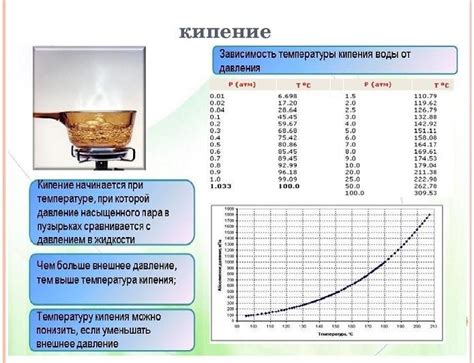
Согласно законам физики, кипение происходит при определенной температуре, называемой температурой кипения. Но эта температура может изменяться в зависимости от давления, под которым находится жидкость.
В обычных условиях, при атмосферном давлении, вода начинает кипеть при температуре 100 градусов Цельсия. Однако, если вода находится в закрытом сосуде и подвергается повышенному давлению, то ее температура кипения увеличивается.
Взаимосвязь между давлением и температурой кипения объясняется тем, что под давлением молекулы жидкости сжимаются и подвергаются большей силе, которую они должны преодолеть, чтобы выпрыгнуть на поверхность жидкости и стать частью пара. Таким образом, для их перехода в газообразное состояние требуется более высокая тепература.
Следует отметить, что данная зависимость является обратной: с увеличением давления температура кипения жидкости повышается, а с его уменьшением - снижается.
Изменение температуры кипения в зависимости от давления имеет практическое значение. Например, при приготовлении пищи в высокогорных условиях, где атмосферное давление ниже, вода начнет кипеть уже при более низкой температуре, что может влиять на процесс готовки.
Исследование зависимости температуры кипения от давления позволяет лучше понять физические свойства веществ и применять эту информацию в различных областях науки и техники.
Как внешнее давление влияет на температуру кипения?

Для понимания этого эффекта можно провести простой эксперимент с кипячением воды. Если мы увеличим внешнее давление, например, использовав плотно закрытую емкость, вода будет кипеть при более высокой температуре, чем при атмосферном давлении. Если же давление уменьшить, кипение начнется при более низкой температуре.
Это явление объясняется законом Лейбница-Клапейрона, который составляет связь между давлением, объемом и температурой газа. При увеличении давления, частицы вещества оказываются более сжатыми, что приводит к повышению энергии коллизий и, соответственно, к повышению температуры кипения.
Наоборот, при уменьшении давления, частицы вещества более распространены и имеют меньшую среднюю энергию. Это приводит к снижению энергии коллизий и, следовательно, к снижению температуры кипения.
Применение этого эффекта возможно в различных областях. Например, в высокогорных условиях, где атмосферное давление ниже, вода начинает кипеть при нижних температурах. Это может создавать определенные трудности в приготовлении пищи или использовании паровой турбины. Температура кипения также влияет на процессы сублимации и обратной конденсации, которые используются в таких областях, как фармакология и физика.
| Давление | Температура кипения воды (°C) |
|---|---|
| Атмосферное давление | 100 |
| Пониженное давление | ниже 100 |
| Повышенное давление | выше 100 |
Таким образом, внешнее давление играет важную роль в изменении температуры кипения вещества. Понимание этого явления позволяет прогнозировать и контролировать различные процессы, связанные с кипением.
Изменение точки кипения при изменении давления

Температура, при которой жидкость начинает кипеть и переходит в газообразное состояние, называется точкой кипения. Однако, внешнее давление может оказывать значительное влияние на этот процесс. При изменении давления, точка кипения жидкости также изменяется.
Обычно при повышении давления точка кипения жидкости также повышается. Это объясняется тем, что вода, как и многие другие вещества, имеет свойство сжиматься при повышении давления. Поэтому, чтобы перейти в газообразное состояние, молекулам жидкости нужно преодолеть больше силы притяжения между собой.
Следовательно, когда точка кипения повышается, жидкость будет кипеть при более высоких температурах. Например, на высоте, где атмосферное давление ниже, вода будет кипеть при более низкой температуре, чем на уровне моря.
С другой стороны, при снижении давления точка кипения также снижается. Уменьшение давления делает молекулы жидкости менее плотными, что позволяет им более свободно двигаться и переходить в газообразное состояние при более низких температурах.
Интересно отметить, что на эксплуатацию парового отопительного котла может оказывать влияние высота над уровнем моря, поскольку точка кипения воды будет отличаться на разных высотах. Как правило, чем выше высота, тем менее эффективной может оказаться работа парового котла из-за снижения точки кипения воды.
Причины изменения температуры кипения в зависимости от давления
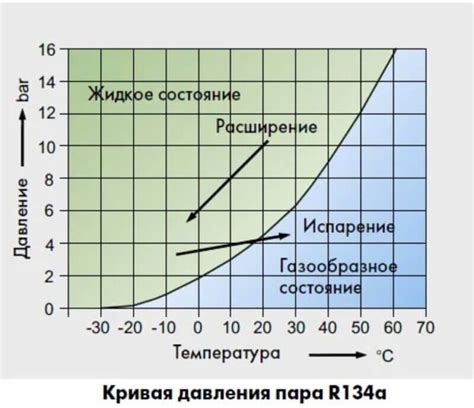
- Увеличение давления приводит к повышению температуры кипения вещества. Это объясняется законом Лей-Шатлеза, который утверждает, что с повышением давления температура кипения также повышается. При увеличении давления молекулы вещества находятся под большим давлением и более трудно покидают жидкую фазу и переходят в газообразную. Таким образом, для перехода в газообразное состояние, молекулам вещества требуется большее количество энергии, что проявляется в повышении температуры кипения.
- Знание изменения температуры кипения в зависимости от давления имеет практическое значение. Например, при приготовлении пищи, давление в кастрюле может изменяться, что влияет на время приготовления и структуру продукта. Также, в промышленности знание этого явления может быть использовано при разработке процессов очистки, производства или синтеза различных веществ.
- Также, изменение температуры кипения в зависимости от давления может быть использовано в научных исследованиях для изучения свойств веществ и их реакций под различными условиями. Это позволяет лучше понять особенности и поведение материалов при различных давлениях и температурах.
- Следует отметить, что изменение температуры кипения вещества в зависимости от давления является обратимым процессом. При снижении давления температура кипения будет уменьшаться. Это можно наблюдать при приготовлении пищи в высокогорных регионах, где сниженное атмосферное давление приводит к раннему кипению воды.
Таким образом, понимание причин изменения температуры кипения в зависимости от давления позволяет использовать это явление в различных областях науки и техники, а также в повседневной жизни для оптимизации различных процессов и улучшения качества продуктов.
Влияние давления на температуру кипения

Однако, температура кипения может изменяться в зависимости от внешнего давления, которое действует на вещество. Правило гласит: при повышении давления, температура кипения тоже повышается, а при снижении давления, температура кипения снижается. Этот феномен объясняется законом Гей-Люссака.
Закон Гей-Люссака гласит, что при постоянном составе вещества и при постоянном объеме внешний давление пропорционально абсолютной температуре. Это значит, что при увеличении внешнего давления абсолютная температура, при которой вещество переходит в состояние пара (кипит), также увеличивается.
Этот эффект может быть использован в различных областях, таких как химия, физика и промышленность. Например, при повышенных давлениях можно достичь кипения вещества при более низкой температуре, что может быть полезно при повышенных требованиях к сохранности материалов и процессах, требующих точного контроля.
Таким образом, влияние давления на температуру кипения является важным физическим явлением, которое необходимо учитывать при проведении экспериментов и проектировании различных процессов, в которых участвуют фазовые переходы вещества.



