Оксид азота 1, или азотистый оксид, является важным химическим соединением, которое широко применяется в различных отраслях науки и промышленности. Он обычно образуется при горении топлива при высоких температурах или в результате биологических процессов, таких как сожжение древесины или метаболизм живых организмов. Несмотря на свою активность в других реакциях, оксид азота 1 не реагирует с кислородом, хотя может показаться логичным, что два из самых распространенных элементов в атмосфере должны взаимодействовать между собой.
Один из основных факторов, почему оксид азота 1 не реагирует с кислородом, заключается в их химической природе и строении. Оксид азота 1 представляет собой особую молекулу, состоящую из атома азота и атома кислорода, связанных одной силой. Эта химическая связь является очень сильной и стабильной, поэтому оксид азота 1 редко разлагается на составляющие его элементы.
Кислород, в свою очередь, имеет другую структуру и свойства. У молекулы кислорода есть две связи между атомами, которые гораздо слабее, чем связь в молекуле оксида азота 1. Поэтому, при контакте с оксидом азота 1, связи кислорода склонны легко разрываться, а сам кислород идет на другие реакции, а не на взаимодействие с молекулой оксида азота 1.
Влияние оксида азота 1 на реакцию с кислородом

Оксид азота 1 (NO) обладает некоторыми особенностями, которые влияют на его реакцию с кислородом (O2). При обычных условиях NO не реагирует напрямую с кислородом, и эта особенность связана с его химической структурой и электронной конфигурацией.
Молекула оксида азота 1 состоит из атома азота и атома кислорода, соединенных двойной связью. Азот имеет электронную конфигурацию 1s2 2s2 2p3, а кислород - 1s2 2s2 2p4. Наличие π-электронной связи в молекуле NO делает ее особенно стабильной и малоактивной.
Реакция NO с кислородом может происходить только при наличии катализаторов или при повышенной температуре и давлении. Катализаторы облегчают разрыв π-связи и инициируют реакцию между NO и O2. Это может быть полезно, например, в промышленных процессах, где требуется получение нитрозных соединений.
Однако, в нормальных условиях, NO обычно взаимодействует с другими реагентами, такими как кислород-водородные соединения или сами NO2 и N2O4. Такие реакции могут приводить к образованию различных азотсодержащих соединений, которые играют важную роль в атмосферной химии и экологии.
Таким образом, оксид азота 1 имеет специфические свойства, которые не позволяют ему реагировать с обычным кислородом. Однако, при определенных условиях, можно создать реакции с его участием, что открывает широкие перспективы для использования данного соединения в различных областях науки и промышленности.
Химическое вещество оксид азота 1

Однако, оксид азота 1 не реагирует с кислородом. Это связано с его структурой и электронной конфигурацией. В молекуле N2O, два атома азота связаны с атомом кислорода двумя тройными связями. Такое распределение электронов позволяет молекуле быть стабильной и не реагировать с кислородом. Кроме того, энергия активации для реакции оксида азота 1 с кислородом слишком высока, что делает эту реакцию маловероятной.
Несмотря на то, что оксид азота 1 сам не реагирует с кислородом, он может быть включен в химические реакции, в которых участвуют другие вещества. Например, оксид азота 1 может служить окислителем или редуктором в реакциях с другими соединениями. Он также может участвовать в образовании смешанных оксидов азота при взаимодействии с другими оксидами азота.
| Свойство | Описание |
|---|---|
| Молекулярная формула | N2O |
| Молярная масса | 44.013 г/моль |
| Плотность | 1.977 г/литр (при 0°C и 1 атм) |
| Точка кипения | -88.48°C |
| Точка плавления | -90.86°C |
| Растворимость | Растворим в воде |
Оксид азота 1 в атмосфере

В атмосфере оксид азота 1 образуется в результате нескольких естественных процессов, таких как грозы, вулканическая активность и молнии. Кроме того, большое количество NO также выделяется в результате антропогенной деятельности, такой как выбросы из автомобилей и промышленных процессов.
Однако оксид азота 1 обычно не реагирует непосредственно с кислородом в атмосфере. Это связано с тем, что NO имеет высокую энергию связи, что делает его малореактивным. Кислород, находящийся в воздухе, обычно не образует стабильные химические связи с NO, поэтому прямая реакция между ними не происходит.
Вместо этого, оксид азота 1 подвергается реакциям в атмосфере, которые приводят к его превращению в другие формы оксидов азота, такие как азота диоксид (NO2). Эти процессы обычно связаны с фотохимическими реакциями и участием других реактивных веществ, таких как пероксиацилние радикалы (ООА) и озон (О3).
Таким образом, хотя оксид азота 1 не реагирует непосредственно с кислородом в атмосфере, его наличие и последующие реакции играют важную роль в образовании других оксидов азота и участвуют в формировании химического состава атмосферы.
Неактивность оксида азота 1 с кислородом

Оксид азота 1 (NO) известен своей неактивностью при реакции с кислородом (O2), что отличает его от других азотистых оксидов. Это объясняется особым строением и химическим свойством NO.
Оксид азота 1 представляет собой двуатомную молекулу, состоящую из одного атома азота (N) и одного атома кислорода (O). Эта молекула очень стабильна и обладает достаточно высокой энергией связи. В то же время, молекула кислорода (O2) представляет собой диатомный газ, состоящий из двух атомов кислорода, также обладающий высокой энергией связи.
Однако, несмотря на высокую энергию связи в молекуле NO, её активность при реакции с кислородом значительно ниже, чем у других азотистых оксидов, таких как оксид азота 2 (NO2). Это обусловлено наличием у NO устойчивого электронного строения и отсутствием несвязанных электронных пар. Такое строение делает молекулу NO менее склонной к реакции с другими веществами.
Кроме того, оксид азота 1 обладает слабым окислительным свойством, которое недостаточно для активной реакции с кислородом. В реакции с кислородом, NO при участии катализаторов может претерпеть окисление до NO2. Данная реакция имеет важное значение в атмосферной химии, так как одним из продуктов этой реакции является атмосферный азотистый оксид, который влияет на качество воздуха и экологическую ситуацию.
Таким образом, неактивность оксида азота 1 с кислородом обусловлена его строением и химическими свойствами, что отличает его от других азотистых оксидов и придает ему особое значение в химии и экологии.
Молекулярная структура оксида азота 1

Оксид азота 1, также известный как динитроген оксид или азотисто-окисный газ, химическая формула которого N2O, представляет собой составной газ, состоящий из двух атомов азота и одного атома кислорода.
Молекула оксида азота 1 имеет линейную геометрию, где оба атома азота связаны с атомом кислорода. Оксид азота 1 является нейтральным соединением и обладает соединительными электронами, которые помогают ему образовывать связи с другими молекулами.
Важно отметить, что оксид азота 1 не реагирует с кислородом, так как уже содержит атом кислорода в своей структуре. Это означает, что оксид азота 1 не может участвовать в химических реакциях, в которых требуется добавление или удаление атомов кислорода.
Оксид азота 1 широко используется в медицинской практике, например, в качестве анестетика или средства для облегчения боли. Он также применяется в пищевой промышленности как аэрозольное вещество, способствующее образованию пены или газирования напитков.
Изучение молекулярной структуры оксида азота 1 позволяет лучше понять его свойства и химическую реактивность. Это познание имеет важное значение для разработки новых методов использования оксида азота 1 в различных областях, включая медицину и пищевую промышленность.
Химические свойства оксида азота 1
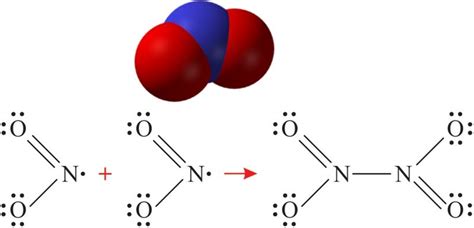
Оксид азота 1, также известный как азотистый оксид, обладает рядом химических свойств, которые делают его уникальным в мире химии.
Устойчивость: Оксид азота 1 обладает высокой устойчивостью и не реагирует с кислородом при нормальных условиях. Это обусловлено особой структурой молекулы и электронной конфигурацией атомов азота и кислорода.
Отсутствие реакции с кислородом: Оксид азота 1 не реагирует с кислородом, поскольку степень окисления азота в этом соединении уже находится на максимальном уровне. Кислород не может передать дополнительные электроны азоту, чтобы произошла химическая реакция.
Реакция с другими веществами: Оксид азота 1 может реагировать с некоторыми другими веществами, включая аммиак и некоторые кислоты. Однако эти реакции происходят под определенными условиями и требуют наличия катализаторов или изменения температуры и давления.
Роль в атмосфере: Оксид азота 1 является одним из главных газов, влияющих на состав атмосферы. Взаимодействие оксида азота 1 с другими веществами, присутствующими в атмосфере, может приводить к образованию других вредных соединений, таких как смог и кислотные дожди.
В целом, химические свойства оксида азота 1 определяют его уникальное поведение и роль в химических процессах и природных явлениях.
Роль оксида азота 1 в биологических процессах
Вазодилатация: Одним из важных свойств оксида азота 1 является его способность расширять кровеносные сосуды. Он работает как сигнальное вещество, которое помогает регулировать сосудистый тонус и кровяное давление. Отсутствие оксида азота 1 может привести к сужению сосудов и возникновению проблем с циркуляцией крови.
Нейротрансмиссия: Оксид азота 1 также имеет важное значение в нервной системе организма. В нервных клетках, он выполняет роль нейромедиатора, передающего сигналы между нервными клетками. Оксид азота 1 помогает регулировать синаптическую активность и способствует передаче нервных импульсов.
Иммунная функция: В иммунной системе, оксид азота 1 играет роль молекулярного сигнала, который активирует и регулирует функцию иммунных клеток. Он может быть высвобожден в ответ на инфекции и воспаление, и помогает в борьбе с патогенами и поддержании иммунной системы в оптимальном состоянии.
Коммуникация между клетками: Оксид азота 1 также участвует в коммуникации между клетками. Он может быть высвобожден одной клеткой и действовать как сигнал для соседних клеток, ответные на что последние могут изменить свое поведение или функционирование в результате этого сигнала. Такая коммуникация может быть важным компонентом разных биологических процессов.
В целом, оксид азота 1 является молекулой, широко распространенной в организмах, играющей важную роль в регуляции и поддержании различных физиологических процессов. Его влияние на сосуды, нервную систему, иммунную функцию и клеточную коммуникацию делает его неотъемлемым компонентом здоровья и хорошего функционирования организма.
Оксид азота 1 в медицине

Оксид азота 1 (N2O), также известный как смехотворный газ, широко используется в медицине благодаря своим анальгетическим и седативным свойствам. Медицинский газ N2O применяется для облегчения боли и снижения тревожности у пациентов.
Оксид азота 1 расслабляет гладкую мускулатуру, что помогает уменьшить мышечные судороги и снизить болевые ощущения у пациентов во время медицинских процедур. Он широко используется в стоматологии, акушерстве и для проведения небольших хирургических вмешательств, таких как удаление зуба или маленькие операции.
Важно отметить, что оксид азота 1 должен использоваться только под медицинским наблюдением, так как неправильное использование или длительное воздействие на организм может вызвать серьезные побочные эффекты. Медицинский персонал должен строго контролировать дозировку и применение этого газа, чтобы обеспечить безопасность пациента.
Перед использованием N2O в медицинских целях необходимо рассмотреть все возможные противопоказания и проконсультироваться с соответствующими специалистами.
Взаимодействие оксида азота 1 с другими веществами

Взаимодействие оксида азота 1 с другими веществами зависит от его реакционной способности и химических свойств.
Оксид азота 1 обычно не реагирует с кислородом, так как образует стабильное соединение NO, которое воздействием с кислородом не подвергается дальнейшим химическим реакциям.
Однако, оксид азота 1 может взаимодействовать с другими веществами, такими как вода и аммиак.
При взаимодействии с водой оксид азота 1 образует азотную кислоту (HNO3), которая является одним из основных компонентов дождевых кислот.
С аммиаком оксид азота 1 может реагировать, образуя соляную кислоту (HCl) и азотистоводородную кислоту (HNO2).
Таким образом, оксид азота 1 может взаимодействовать с другими веществами, образуя различные соединения, которые могут иметь физические и химические последствия для окружающей среды.
Продукты реакции оксида азота 1 с кислородом

Однако, оксид азота 1 может быть вовлечен в другие химические реакции с кислородом. Например, в атмосферных условиях оксид азота 1 может реагировать с кислородом в аэрозолях и образовывать нитраты, которые являются важными компонентами атмосферного цикла азота.
Кроме того, оксид азота 1 также может быть вовлечен в реакции с кислородом в присутствии катализаторов, таких как металлы или другие соединения. В результате таких реакций могут образовываться другие оксиды азота, такие как диоксид азота (NO2) или триоксид азота (N2O3), которые являются более активными оксидами азота и способны реагировать с кислородом более интенсивно.
Таким образом, хотя оксид азота 1 не реагирует с кислородом прямым окислением, он может быть вовлечен в другие химические реакции с кислородом, образуя нитраты или другие оксиды азота. Эти реакции играют важную роль в атмосферной химии и могут приводить к образованию различных важных веществ в атмосфере.
Исследования оксида азота 1 и его реакции с кислородом

Исследования свойств оксида азота 1 и его реакции с кислородом проводятся в химических лабораториях и научных центрах с целью понять физико-химические особенности этого соединения. Изучение реакций между оксидом азота 1 и кислородом может помочь улучшить процессы сжигания топлива и снизить выбросы вредных веществ в атмосферу.
Одной из основных причин, по которой оксид азота 1 не реагирует с кислородом, является его высокая стабильность. При комнатной температуре и давлении оксид азота 1 обычно представлен в виде двухатомных молекул N2O2, которые трудно разрушить. Кроме того, реакция между азотной кислотой и кислородом требует высоких энергий активации и специфических условий.
Хотя спонтанная реакция между оксидом азота 1 и кислородом является крайне маловероятной, при определенных экстремальных условиях, таких как высокие температуры и наличие катализаторов, возможны реакции между этими веществами. Такие условия обычно возникают в промышленных процессах, сжигании топлива или в результате молнии в атмосфере. В этих случаях образующиеся соединения могут быть опасными для окружающей среды, поэтому исследование этих реакций имеет важное значение для понимания и контроля выбросов вредных веществ.
| Симбол | Название |
|---|---|
| N2O2 | Оксид азота 1 |
| O2 | Кислород |



