Нулевая группа благородных газов - это особая категория химических элементов, включающая в себя гелий, неон, аргон, криптон, ксенон и радон. Название "благородные газы" они получили благодаря своей малоактивности и инертности. Однако, нулевая группа благородных газов отличается особыми свойствами, которые полностью оправдывают ее место в периодической системе элементов.
Первая причина обоснования нулевой группы благородных газов - их совершенная электронная конфигурация. Благодаря наполнению внешней оболочки электронами, эти элементы обладают полностью заполненными s- и p-оболочками. Такая конфигурация делает их электронно устойчивыми и практически неактивными во взаимодействиях с другими химическими элементами. Именно поэтому гелий, неон и другие газы нулевой группы зачастую используются в технике и науке для создания атмосфер инертных газов.
Вторая причина заключается в их низкой реактивности и химической стабильности. Благородные газы практически не вступают в химические реакции с другими веществами, так как у них отсутствуют непарные электроны во внешней оболочке. Неон, например, является весьма устойчивым элементом, который не образует химические связи и остается инертным даже при высоких температурах. Это свойство благородных газов делает их незаменимыми в различных отраслях научных и технических исследований, включая оптическую электронику.
Преимущества благородных газов

Благородные газы представляют ряд преимуществ, которые делают их уникальными и необходимыми во многих областях нашей жизни:
| Высокая химическая инертность | Благородные газы обладают высокой химической инертностью, что означает, что они почти не реагируют с другими веществами. Это позволяет им использоваться во многих промышленных процессах, например, в производстве полупроводников, где высокая чистота газов критична для получения качественных изделий. |
| Отличные теплофизические свойства | Благородные газы обладают высокой теплопроводностью, что делает их незаменимыми в некоторых технических и научных приложениях. Они эффективно переносят тепло и способствуют регулировке температуры в многих системах и устройствах, таких как терморегуляторы, кондиционеры и холодильники. |
| Безопасность использования | Благородные газы являются безопасными для использования благодаря своей низкой реактивности и стабильности. Они не обладают токсичностью и взрывоопасностью, что делает их безопасными для работы в различных условиях и средах. |
| Устойчивость к окружающим условиям | Благородные газы обладают высокой устойчивостью к окружающим условиям, таким как высокие и низкие температуры, атмосферное давление и влажность. Это делает их незаменимыми в приложениях, где необходима стабильность работы, например, в автомобильной промышленности, аэрокосмической отрасли и медицине. |
| Широкий спектр применения | Благородные газы нашли применение во многих различных отраслях, начиная от науки и исследований, и заканчивая промышленностью и медициной. Они используются в качестве рабочих сред в газоанализаторах, в процессах сварки и резки металлов, в медицинских аппаратах и инструментах, и многих других областях, где их свойства ценятся и необходимы. |
Особенности благородных газов

Один из главных аргументов в пользу принятия нулевой группы благородных газов в периодическую систему элементов – это их способность необразовывать нестабильные соединения. Благодаря этому, благородные газы эффективно используются в промышленности и научных исследованиях.
Кроме того, благородные газы обладают высокой стабильностью и безопасностью. Они не являются токсичными и не взрывоопасны, что делает их безопасными для использования в различных отраслях промышленности, включая медицину, энергетику и электронику.
Благородные газы также обладают свойством растворяться в различных веществах, что позволяет использовать их в разных процессах сепарации, очистки и синтеза. Например, гелий широко применяется в газовой хроматографии для разделения и идентификации различных веществ.
Наконец, благородные газы обладают высокими теплопроводностью и электропроводностью. Эти свойства делают их важными компонентами в различных технологиях, включая электронику и светотехнику. Например, аргон используется в заполнителях для ламп накаливания и газовых разрядных трубок.
Исторический аспект

Процесс открытия и изучения нулевой группы благородных газов начался в конце XIX века. Основными исследователями этой области были ученые Анри Моиссан и Лоренцо Гассман. Они провели ряд экспериментов и наблюдений, которые позволили установить некоторые свойства этих газов.
Первым благородным газом, открытым учеными, был гелий. В 1868 году французский астроном Жюль Жансен открыл неизвестный элемент в спектре слепой пятна на солнечном диске. Позже он был независимо открыт в Земной атмосфере и получил название гелий. Этот элемент был классифицирован как газ и добавлен в нулевую группу благородных газов.
Последующие исследования привели к открытию других элементов нулевой группы, таких как неон, аргон, криптон и ксенон. Вместе эти элементы обладают сходными свойствами: они практически не реагируют с другими элементами, обладают низкой положительной электроотрицательностью, не имеют окрашивающих свойств и характеризуются низкой растворимостью в воде. Эти свойства делают их идеальными для использования в научных и промышленных целях.
С учетом этих исследований в 1962 году была обоснована нулевая группа благородных газов. Эти элементы были выделены в отдельный раздел таблицы химических элементов и получили специальное место в системе классификации.
Химические свойства благородных газов
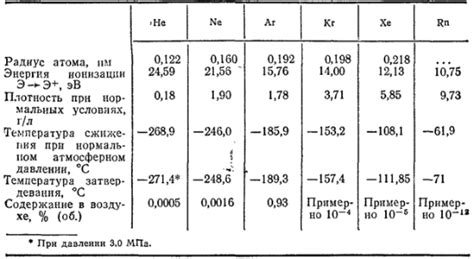
Благородные газы, такие как гелий, неон, аргон, криптон, ксенон и радон, обладают рядом уникальных химических свойств, которые делают их особенно ценными и полезными в различных областях.
1. Практически неподвижные: Благородные газы являются стабильными и практически неподвижными, что означает, что они мало взаимодействуют с другими веществами. Это делает их невоспламеняемыми и не реагирующими с большинством других элементов. Именно благодаря этим свойствам они иногда называются "неподвижными газами".
2. Необычные соединения: В то время как благородные газы обычно не реагируют с другими элементами, существуют некоторые условия, при которых они могут образовывать необычные соединения. Например, ксенон может образовывать соединения с некоторыми химическими элементами, такими как фтор, ионит или платина.
3. Исключительная благородность: Название "благородные газы" происходит от их благородного поведения и стабильности. Эти газы обычно не реагируют с другими веществами, что делает их идеальными для использования в процессах, требующих незатухающего тепла или защиты от окисления.
4. Охлаждающие свойства: Благородные газы, такие как гелий и криптон, имеют очень низкую температуру кипения, что делает их идеальными для использования в охлаждающих системах. Они могут быть использованы для создания экстремально низких температур или как охлаждающие агенты для электроники, лазеров и других технологий.
5. Применение в осветительной технике: Благородные газы, такие как неон, криптон и ксенон, обладают способностью излучать яркий свет различных цветов при пропускании через них электрического тока. Именно благодаря этому свойству они широко применяются в осветительной технике для создания рекламных вывесок, неоновых светильников и фар автомобилей.
Важность благородных газов в промышленности

Благородные газы, такие как гелий, неон, аргон, криптон и ксенон, играют важную роль в промышленности. Их уникальные свойства и специфические характеристики делают эти газы не заменимыми во многих процессах и областях деятельности.
Прежде всего, благородные газы обладают стабильностью и низкой химической активностью. Это позволяет им применяться в различных видов промышленности, где требуется инертность газа. Например, аргон широко используется в процессе сварки и резки металлов, так как его присутствие в атмосфере предотвращает окисление металлов и повышает качество сварочного шва.
Благородные газы также отличаются отличной электрической изоляцией. Их использование визионеры предпочитают использовать для заполнения ламп высокого давления, в том числе длагородные газы использоваться в газоразрядных лампах, таких как неоновые и криптоновые лампы, а также в осветительных приборах, где требуется стабильность и долговечность.
Кроме того, благородные газы также применяются в производстве электроники и полупроводников. Гелий, например, используется в контролируемом процессе охлаждения при создании суперпроводников и других чувствительных приборов. А аргон используется в сфере лазерных технологий и вакуумной техники, где его низкое теплопроводность и высокая стабильность имеет большое значение.
- Благородные газы также находят применение в:
- Медицине, в частности в хирургии и дыхательной аппаратуре, где гелий и ксенон используются как анестетики;
- Производстве стекла и оптики, где благородные газы применяются в процессе создания прозрачных и высококачественных материалов;
- Производстве пищевой продукции, так как гелий может использоваться для сохранения свежести и предотвращения окисления пищевых продуктов.
Таким образом, благородные газы имеют обширное практическое применение в различных отраслях промышленности. Их уникальные свойства делают их неотъемлемой частью многих процессов и обеспечивают безопасность, качество и эффективность во многих сферах деятельности.
Проблемы и вызовы исследования благородных газов

Исследование благородных газов представляет собой сложную и трудоемкую задачу, связанную с множеством проблем и вызовов. Несмотря на их высокую химическую стабильность и инертность, благородные газы имеют свои особенности, которые требуют детального изучения.
Одной из проблем, с которыми сталкиваются исследователи, является достаточно высокая стоимость благородных газов. Это делает проведение экспериментов и обширные исследования чрезвычайно затратными. Кроме того, они являются ограниченным ресурсом и не могут быть воспроизведены искусственным путем в неограниченном количестве.
Еще одной проблемой является сложность сбора и анализа данных благородных газов. В силу их малой концентрации в атмосфере и низкой растворимости в водных средах, требуется применение специальных методов и инструментов для их обнаружения и измерения. Это требует высокой точности и чувствительности приборов, а также специализированных навыков и опыта у исследователей.
Дополнительной сложностью является малая активность благородных газов в химических реакциях. Они редко образуют соединения с другими элементами, что затрудняет изучение их химических свойств и взаимодействий. Для этого требуются специализированные условия и методы, которые сложны в реализации.
Также стоит отметить, что благородные газы имеют важное применение в различных сферах, включая научные исследования, медицину, производство полупроводников и другие. Их использование требует тщательного контроля и оптимизации процессов с целью экономии и улучшения эффективности.
В свете всех этих проблем и вызовов, исследование благородных газов является актуальной и значимой задачей, требующей внимания и усилий со стороны научного сообщества.
Обоснование нулевой группы благородных газов

Причина обоснования нулевой группы благородных газов лежит в особенностях электронной структуры данных элементов. Атомы благородных газов имеют полностью заполненные энергетические оболочки. Это означает, что внешнее s-подуровень содержит максимальное количество электронов.
Такая электронная конфигурация является основным фактором, определяющим стабильность и инертность благородных газов. Благородные газы не образуют химических связей с другими элементами и практически не участвуют в химических реакциях.
Инертность благородных газов обусловлена тем, что заполненность электронных оболочек создает полный набор электронов, который удовлетворяет принципу экономии энергии. Атомы благородных газов не стремятся к образованию химических связей, так как при этом возникают нераспределенные электронные пары, что приводит к нестабильности системы электронов.
| Элемент | Атомный номер | Электронная конфигурация |
|---|---|---|
| Гелий (He) | 2 | 1s2 |
| Неон (Ne) | 10 | 1s2 2s2 2p6 |
| Аргон (Ar) | 18 | 1s2 2s2 2p6 3s2 3p6 |
| Криптон (Kr) | 36 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 |
| Ксенон (Xe) | 54 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 |
| Радон (Rn) | 86 | 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 |
Благородные газы имеют широкое применение в различных отраслях науки и промышленности. Например, гелий используется в анализе газов и шариковых аэростатах, аргон применяется в сварочных работах и в процессе зашиты металлов от окисления.
Таким образом, обоснование нулевой группы благородных газов заключается в их уникальной электронной структуре, обеспечивающей высокую степень стабильности и инертности.
Свойства благородных газов
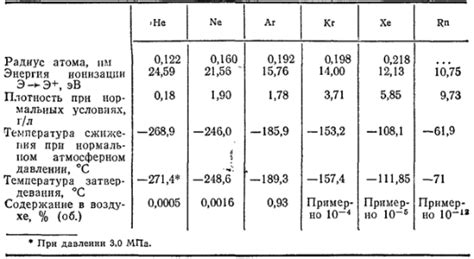
1. Инертность:
Благородные газы отличаются высокой инертностью, то есть они обладают малой реакционной способностью. Это связано с тем, что у них полностью заполнена внешняя энергетическая оболочка, что делает их стабильными и малоактивными химическими элементами.
2. Низкая температура кипения и плавления:
Благородные газы имеют очень низкую температуру кипения и плавления. Например, хлор интенсивно кипит при температуре –34 °C, а криптон плавится при температуре –156,6 °C. Это делает благородные газы удобными для использования в разных областях технологии и научных исследованиях.
3. Высокая плотность:
Благородные газы обладают высокой плотностью. Например, ксенон имеет плотность 5,9 г/л, что делает его одним из самых плотных газов в природе. Это свойство благородных газов позволяет использовать их в различных технических и промышленных процессах.
4. Безцветность и отсутствие запаха:
Благородные газы обычно являются безцветными и не имеют запаха. Это делает их очень удобными для использования в подразделениях медицины и промышленности, где требуется чистый и непахучий газ.
5. Высокая стоимость и редкость:
Благородные газы являются редкими элементами на Земле. Их добыча и производство требуют сложных технологических процессов, что делает их дорогими. Из-за своей редкости и ценности, благородные газы применяются в основном в высокотехнологичных отраслях и научных исследованиях.
Все эти свойства делают благородные газы особенными и важными для различных отраслей науки и техники.
Применение благородных газов в медицине

Благородные газы, такие как гелий, аргон, неон и криптон, обладают уникальными свойствами, которые находят широкое применение в медицине. В сочетании с их инертностью и низкой реактивностью, эти газы стали неотъемлемой частью современных медицинских технологий.
Гелий, например, обладает очень низкой плотностью, что делает его идеальным для использования в дыхательных смесях для пациентов, страдающих отдышкой и заболеваний легких. Гелий облегчает дыхание, уменьшает сопротивление воздушных путей и улучшает кислородообмен в организме.
Аргон широко применяется в медицине для охлаждения. Благодаря своей низкой температуре кипения (-185.7°C), аргон может использоваться для охлаждения ран и опухолей, что помогает снизить воспаление, облегчить боль и способствовать быстрому выздоровлению.
Неон и криптон, благодаря своим особенностям свечения, нашли свое применение в медицинских приборах для диагностики и лечения. Например, неоновые и криптоновые лазеры используются для хирургических операций, удаления опухолей и обработки урологических заболеваний.
Использование благородных газов в медицине продолжает активно развиваться. Каждый год появляются новые технологии и методы применения этих газов для повышения эффективности и комфорта врачебных процедур. Благодаря своим уникальным свойствам, благородные газы становятся незаменимым инструментарием в борьбе с различными болезнями и патологиями.
Экологическая значимость благородных газов

Благородные газы, такие как гелий, неон, аргон, криптон и ксенон, играют важную роль в экологических процессах и имеют существенное влияние на окружающую среду. Вот несколько причин, почему эти газы имеют высокую экологическую значимость:
1. Участие в глобальном потеплении и изменении климата: Благородные газы входят в состав парниковых газов, которые способствуют удержанию тепла в атмосфере и вызывают глобальное потепление. Они вносят свой вклад в увеличение температуры Земли и глобальные климатические изменения.
2. Роль в озоновом слое: Благородные газы также являются важными компонентами воздуха и играют важную роль в формировании озонового слоя. Они служат стабилизаторами химических процессов, которые приводят к разрушению озона и создают угрозу для живых организмов на Земле. Сокращение содержания этих газов воздухе может иметь серьезное отрицательное воздействие на озоновый слой и усилить его разрушение.
3. Использование в энергетической отрасли: Благородные газы играют важную роль в энергетической отрасли и находят применение в газовых турбинах и других технологиях для производства энергии. Они позволяют увеличить эффективность процессов сжигания и снизить выбросы загрязняющих веществ, что способствует снижению негативного воздействия на окружающую среду.
4. Использование в научных исследованиях: Благородные газы широко применяются в научных исследованиях и в различных научных областях, таких как физика, химия и астрономия. Они используются в специализированных лабораториях и оборудовании для проведения экспериментов и изучения различных физических и химических процессов.
Таким образом, благородные газы имеют не только научное и технологическое значение, но и значительное влияние на окружающую среду. Понимание свойств и роли этих газов помогает нам разработать эффективные меры для поддержания экологического баланса и снижения негативного воздействия на окружающую среду.



